
| A、2A(l)+B (l)═2C(g)△H1 |
| B、2A(g)+B (g)═2C(g)△H2 |
| C、2A(g)+B ( g )═2C(l)△H3 |
| D、2A(l)+B (l)═2C(l)△H4 |


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
| A、16g | B、23.4g |
| C、31g | D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②>④>③>① |
| B、②>④>①>③ |
| C、③>①>②>④ |
| D、①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A2+2B2=2AB2 |
| B、2A2+B2=2A2B |
| C、3A2+B2=2A3B |
| D、A2+3B2=2AB3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
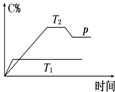 在一定条件下,可逆反应A+B?mC变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
在一定条件下,可逆反应A+B?mC变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用米汤检验食用加碘盐中含有碘 |
| B、用醋、石灰水验证蛋壳中含有碳酸盐 |
| C、用碘酒检验葡萄中是否含有淀粉 |
| D、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、对于任何化学反应来说,反应速率越快,反应现象就越明显 |
| B、化学反应速率为0.8 mol/(L?s)是指1秒钟时某物质的浓度为0.8 mol/L |
| C、根据化学反应速率的大小可以知道化学反应进行的快慢 |
| D、化学反应速率是指一定时间内任何一种反应物物质的量的减少或任何一种生成物物质的量的增加 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com