
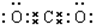 ,D为氨气,因为氨分子中氮原子的价层电子对数为
,D为氨气,因为氨分子中氮原子的价层电子对数为| 5+3 |
| 2 |
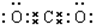 ;三角锥形;
;三角锥形;
| ||
| △ |
| ||
| △ |
| ||
| ||
| ||
| ||
| 4.48L |
| 22.4L/mol |


科目:高中化学 来源: 题型:

| H2O |
| LiAlH4 |
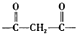 .
.查看答案和解析>>
科目:高中化学 来源: 题型:
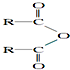
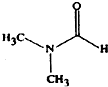 淮南市煤炭年产量已达到1忆吨以上,是我国13个忆吨煤炭生产基地之一.二甲基甲酰胺(C3H7NO)是以煤炭为原料的重要化工产品之一,其结构如图所示,下列关于二甲基甲酰胺的说法不正确的是( )
淮南市煤炭年产量已达到1忆吨以上,是我国13个忆吨煤炭生产基地之一.二甲基甲酰胺(C3H7NO)是以煤炭为原料的重要化工产品之一,其结构如图所示,下列关于二甲基甲酰胺的说法不正确的是( )| A、元素电负性大小为:O>N>C |
| B、B二甲基甲酰胺分子中既含有极性键又含有非极性键 |
| C、二甲基酰胺具有还原性,在化学反应中长做还原剂 |
| D、在空气中完全燃烧73g二甲基甲酰胺可以得到标准状况下67.2LCO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.40mL |
| 第二次 | 3.00mL | 21.10mL |
| 第三次 | 0.20mL | 20.40mL |
| 第四次 | 0.00mL | 18.20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.448L |
| B、0.896L |
| C、4.48L |
| D、8.96L |
查看答案和解析>>
科目:高中化学 来源: 题型:
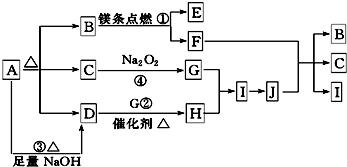
 如图是中学化学常见物质之间的转换关系,其中A、C、D、F、I为单质,其余为化合物,C和D在点燃或者加热的条件下生成淡黄色的固体,B常温下为液态.试回答下列有关问题:
如图是中学化学常见物质之间的转换关系,其中A、C、D、F、I为单质,其余为化合物,C和D在点燃或者加热的条件下生成淡黄色的固体,B常温下为液态.试回答下列有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碘是人体必需的微量元素,所以要多吃富含高碘酸的食物 |
| B、为了增加食物的营养成分,可以大量使用食品添加剂 |
| C、聚乙烯塑料的老化是由于发生了加成反应 |
| D、粮食酒主要经过了淀粉→葡萄糖→乙醇的化学变化过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠在水层中反应并四处游动 |
| B、钠停留在煤油层中不发生反应 |
| C、钠在煤油的液面上反应并四处游动 |
| D、钠在煤油与水的界面处反应并可能作上下跳动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化氢水溶液能导电,所以氯化氢是电解质 |
| B、铜丝能导电,所以铜是电解质 |
| C、固体氢氧化钠不导电,所以氢氧化钠是非电解质 |
| D、SO3溶于水能导电,所以SO3是电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com