
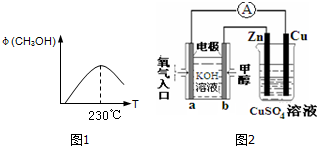
分析 (1)230℃处于平衡状态,再升高温度甲醇的体积分数,说明升高温度平衡向逆反应方向移动;
(2)说明升高温度平衡向逆反应方向移动,平衡常数减小;
(3)参加反应CO为2.5mol×90%=2.25mol,进而计算平衡时混合气体总物质的量,恒温恒容下,压强之比等于物质的量之比;
(4)b电极通入甲醇,发生氧化反应,a电极通入氧气,发生还原反应,则a为正极、b为负极,Cu连接a极,则为阳极,b电极上甲醇失去电子,碱性条件下生成碳酸根离子与水;根据电子转移守恒计算消耗氧气的体积.
解答 解:(1)230℃处于平衡状态,再升高温度甲醇的体积分数,说明升高温度平衡向逆反应方向移动,而升高温度平衡向吸热反应移动,故正反应为放热反应,则△H<0,故答案为:<;
(2)正反应为放热反应,升高温度平衡向逆反应方向移动,平衡常数减小,则K<1,故答案为:<;
(3)参加反应CO为2.5mol×90%=2.25mol,则:
CO(g)+2H2(g)?CH3OH(g) 气体物质的量减小
1 2
2.25mol 4.5mol
故平衡后混合气体总物质的量为2.5mol+7.5mol-4.5mol=5.5mol,恒温恒容下,压强之比等于物质的量之比,此时容器内的压强为开始时的$\frac{5.5mol}{2.5mol+7.5mol}$=0.55倍,
故答案为:0.55;
(4)b电极通入甲醇,发生氧化反应,a电极通入氧气,发生还原反应,则a为正极、b为负极,Cu连接a极,则为阳极,b电极上甲醇失去电子,碱性条件下生成碳酸根离子与水,电极反应式为:CH3OH+8OH--6e-=CO2-3+6H2O;
当铜片的质量变化为12.8g时,消耗的Cu为$\frac{12.8g}{64g/mol}$=0.2mol,根据电子转移守恒可知消耗氧气为$\frac{0.2mol×2}{4}$=0.1mol,则a极上消耗的O2在标准状况下的体积为0.1mol×22.4L/mol=2.24L,
故答案为:阳;CH3OH+8OH--6e-=CO2-3+6H2O;2.24.
点评 本题考查化学平衡计算与影响因素、平衡常数、原电池与电解原理等,难度中等,(4)中注意利用电子转移守恒计算解答.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
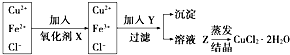 工业上制取纯净的CuCl2•2H2O的主要过程是:
工业上制取纯净的CuCl2•2H2O的主要过程是:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )甲酯并计算其产率.实验步骤如下:
)甲酯并计算其产率.实验步骤如下: 水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
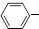 C2H5(g)?
C2H5(g)?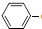 CH=CH2(g)+H2(g)△H=akJ.mol-1.经一段时间后达到平衡.反应过程中测定的部分数据见下表:
CH=CH2(g)+H2(g)△H=akJ.mol-1.经一段时间后达到平衡.反应过程中测定的部分数据见下表:| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(乙苯)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(苯乙烯)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
| A. | 反应在前20 min的平均速率为v(H2)=0.004mol•L-1•min-1 | |
| B. | 保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08mol•L-1,则a<0 | |
| C. | 保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率为50.0% | |
| D. | 相同温度下,起始时向容器中充入0.10mol乙苯、0.10mol苯乙烯和0.30molH2,达到平衡前v(正)>v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
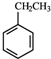 (g)+CO2(g)?
(g)+CO2(g)?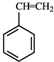 (g)+CO(g)+H2O(g)△H=-166KJ/mol
(g)+CO(g)+H2O(g)△H=-166KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
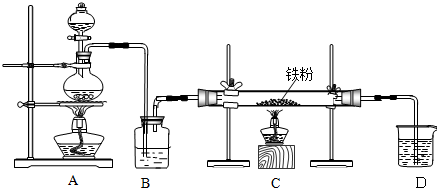
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子层序数越大,s原子轨道的形状相同、半径越大 | |
| B. | 在同一电子层上运动的电子,其自旋方向肯定不同 | |
| C. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| D. | 原子最外层电子排布是5s1的元素,其氢氧化物不能使氢氧化铝溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 各种物质中的少量杂质 | 试剂 | 方法 |
| A | 苯中的溴 | NaOH溶液 | 分液 |
| B | 乙醇中的乙酸 | 浓硫酸 | 加热 |
| C | 乙酸乙酯中的乙酸 | NaOH溶液 | 分液 |
| D | 甲烷中混有乙烯 | 酸性KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com