
【题目】某化学反应2X(g) ![]() Y(g)+Z(g)在4种不同条件下进行,Y、Z起始浓度为0,反应物X的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
Y(g)+Z(g)在4种不同条件下进行,Y、Z起始浓度为0,反应物X的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
化情况如下表:

下列说法不正确的是( )
A. c>1.0 B. 实验2可能使用了催化剂
C. 实验3比实验2先达到化学平衡状态 D. 前10分钟,实验4的平均化学反应速率比实验1的大
科目:高中化学 来源: 题型:
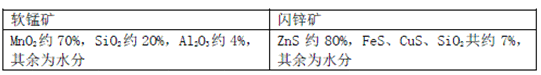
【题目】某地有软锰矿和闪锌矿两座矿山,它们的组成(质量分数)如下:
科研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如下图所示。
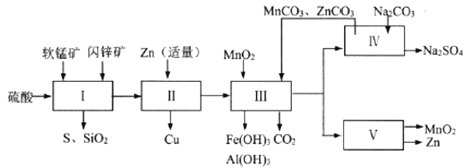
请回答下列问题。
(1)流程I所得滤液中含有MgSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等,则流程I中被氧化的物质有_______种。
(2)流程II中反应的离子方程式为_____________。
(3)氢氧化物开始沉淀的pH如下表:
氢氧化物 | Fe(0H)3 | Al(0H)3 | Fe(0H)2 |
开始沉淀pH | 1.5 | 3.3 | 7.6 |
①流程III中MnO2的作用是将Fe2+氧化成Fe3+,不直接生成Fe(OH)3沉淀的原因是_________。
②MnCO3和ZnCO3的作用是______________。
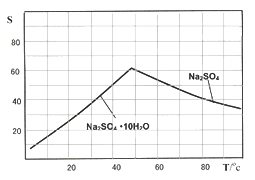
(4)下图是Na2SO4和Na2SO4·10H2O的溶解度(g/100g水)曲线,又知MnCO3和ZnSO4的溶解度随温度的升高而增大,则流程IV得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶、趁热过滤、_____、干燥,要“趁热”过滤的原因是:______________。
(5)本工艺所用的原料除软锰矿、闪锌矿、硫酸外还需要购买的原料是_______。
(6)流程V的反应为:MnSO4+ZnSO4+2H2O ![]() MnO2+Zn+2H2SO4,写出阳极反应式________。
MnO2+Zn+2H2SO4,写出阳极反应式________。
(7)MnO2和Zn可按物质的量之比1 : 1 生产锌-锰干电池,则从主产MnO2和Zn的角度计算,所用软锰矿和闪锌矿的质量比大约是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由两种金属组成的混合物4.8g,跟氯气完全反应时,消耗氯气2.24L(标准状况),则混合物的组成可能是
A. 镁和铁 B. 钠和铁 C. 锌和锅 D. 锌和铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼(B)及其化合物是用途广泛的化工原料,硼可与多种元素形成化合物。
(1)B的价电子轨道表示式为________ 。
(2)BF3与NH3可以通过配位键形成NH3·BF3。
① 基态![]() 原子的核外电子有________种不同的运动状态
原子的核外电子有________种不同的运动状态
② NH3 的键角________CH4的键角(填“大于”、“小于”或“等于”)。BF3为________分子(填“极性”或“非极性”)。
③ 在NH3·BF3所形成的配位键中,________原子提供空轨道。
(3)氮化硼(BN)晶体有多种结构。六方氮化硼与石墨相似,具有层状结构;立方氮化硼与金刚石相似,具有空间网状结构。它们的晶体结构如下图所示。

① 六方氮化硼和立方氮化硼中,B原子的杂化方式分别为_______、_______。
② 六方氮化硼能像石墨一样做润滑剂,原因是_______;但它不能像石墨一样导电,可能的原因是_______.
③ 已知立方氮化硼的晶胞参数(即晶胞的边长)为acm,则立方氮化硼的密度为_______g/cm3(只要求列算式,不必计算出结果,阿伏加德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式如图,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是

A.始祖鸟烯与乙烯互为同系物
B.若Rl=R2= —CH3,则其化学式为C12H16
C.若R1=R2,烯烃双键碳原子上的氢也能取代,则始祖鸟烯环上的二氯代物有10种
D.始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组为探究铜与浓硫酸反应气体产物的性质,拟用下图所示的装置进行实验。

请回答下列问题:
(1)仪器X的名称为_________。
(2)Y溶液可以是________,相应的实验现象是____________________________________________________。
(3)丙装置的作用是______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫酸锰废液(主要含Mn2+、H+、SO42-,还含有少量Cl-、Zn2+、Cu2+)制取金属锰的流程如下:

(1)滤渣I的主要成分是CuCl,潮湿条件下易被空气氧化。过滤I操作时间不宜过长,其原因是_____________(用离子方程式表示)。
(2)若过滤I后所得滤液中Zn2+和Cu2+的浓度均为0.01mol/L,加入(NH4)2S溶液,先析出CuS沉淀,则Ksp(ZnS)_______Ksp(CuS)(填“>”或“<”)。除锌、铜时须控制溶液pH, pH过低,金属离子沉淀不完全,原因是_____________。
(3)写出电解过程中发生反应的化学方程式:_______。若不除去硫酸锰废液中的Cu2+、Zn2+、Cl-,则电解时会导致____________。
(4)向CuCl固体中加入一定量的NaCl溶液,反应过程中各粒子的物质的量随时间变化如图所示。写出该反应过程中的离子方程式:____________(X用对应粒子的化学式表示)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com