
| A. | 钠和钾合金具有导电性,可用作快中子反应堆热交换剂 | |
| B. | 明矾溶于水后能产生Al(OH)3胶体,可用作净水剂 | |
| C. | 水玻璃(Na2SiO3)易溶于水,可用作防火剂 | |
| D. | 浓硫酸具有脱水性,可用于干燥氢气 |
科目:高中化学 来源: 题型:选择题
| A. | 溴水中通入乙烯气体后,颜色会褪去 | |
| B. | 一定条件下,溴水可与氢气发生加成反应 | |
| C. | 乙烯可令酸性高锰酸钾溶液褪色 | |
| D. | 乙烯可燃,完全燃烧后产生CO2和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46g组成为C2H6O的有机物,C-H键数目一定为5NA | |
| B. | 1mol羟基中含有的电子数为10NA | |
| C. | 标准状况下,1mol CCl4的体积约为22.4 L | |
| D. | 14g乙烯和丙烯的混合气体中所含原子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
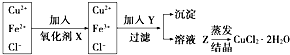
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/L | B. | 0.1mol/L | C. | 4mol/L | D. | 0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 被提纯的物质[括号内物质是杂质] | 除杂试剂 | 反应的离子方程式 | |
| 1 | NaHCO3溶液( Na2CO3) | ||
| 2 | NaCl溶液 (MgCl2) | ||
| 3 | KNO3溶液(KCl) | ||
| 4 | Cu(Mg) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 NH4+(2)
NH4+(2)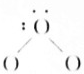 H2O(3)
H2O(3)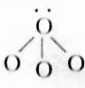 NH3
NH3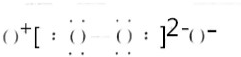 Na2O2(5)
Na2O2(5)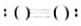 N2
N2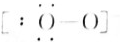 OH-(7)
OH-(7)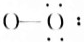 HF.
HF.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com