
| A. | 铜锌原电池中铜是正极 | B. | 用电解法精炼粗铜时粗铜做阳极 | ||
| C. | 在镀件上镀铜时可用金属铜做阳极 | D. | 电解水制H2、O2时铜做阳极 |
分析 A.铜锌原电池中,锌易失电子而作负极,铜作正极;
B.电解精炼粗铜时,粗铜作阳极;
C.电镀时,镀层作阳极,镀件作阴极;
D.阳极上铜失电子生成铜离子.
解答 解:A.铜锌原电池中,锌易失电子发生氧化反应而作负极,铜作正极,正极上得电子发生还原反应,故A正确;
B.电解精炼粗铜时,粗铜作阳极,纯铜作阴极,故B正确;
C.电镀时,镀层作阳极,镀件作阴极,所以在镀件上电镀铜时,铜作阳极,镀件作阴极,故C正确;
D.电解水制H2、O2时,铜不能做阳极,铜作阳极,铜失电子,阳极上得不到氧气,故D错误;
故选D.
点评 本题考查了原电池和电解池原理,题目难度不大,明确各个电极上得失电子是解本题关键,注意活泼金属作电解池阳极时,金属失电子而不是溶液中阴离子失电子,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 将Al条投入NaOH溶液中:Al+4OH-=AlO2-+2H2O | |
| B. | 铜溶于浓硫酸中并加热:Cu+4H++SO42-$\frac{\underline{\;\;△\;\;}}{\;}$Cu2++SO2↑+2H2O | |
| C. | 碳酸氢钙溶液中加入少量氢氧化钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| D. | 向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的稀硫酸:CO32-+H+=HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K(HF)=c(F-)?c(H+)/c(HF ) | B. | K(HNO2)=7.2×10-4 | ||
| C. | 酸性强弱为 HF>HNO2 | D. | K(HNO2)<K(HF) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤ | B. | 只有①④ | C. | 只有②③ | D. | 只有③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而增大有效碰撞的次数 | |
| B. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 | |
| D. | 催化剂不影响反应活化能但能增大单位体积内活化分子的百分数,从而增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在CH3COONa 溶液中滴入无色酚酞,溶液变红:CH3COO-+H2O?CH3COOH+OH- | |
| B. | 在Mg(OH)2白色悬浊液中滴入饱和FeCl3溶液,悬浊液变红褐:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ | |
| C. | 在NaHSO3溶液中滴加紫色石蕊溶液,溶液变红:NaHSO3=Na++H++SO32- | |
| D. | 在草酸溶液中滴入几滴稀H2SO4酸化的KMnO4溶液,溶液无色:2MnO4-+5H2C2O4+6H +=2Mn2++10CO2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 我国规定:室内甲醛含量不得超过0.08mg•m-3.某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛的含量,请你协助他们完成相关学习任务.(部分装置如图),其反应原理及步骤如下:
我国规定:室内甲醛含量不得超过0.08mg•m-3.某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛的含量,请你协助他们完成相关学习任务.(部分装置如图),其反应原理及步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag得到电子 | B. | X为AgS | ||
| C. | O2被还原 | D. | 每生成1 mo1X转移电子数4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
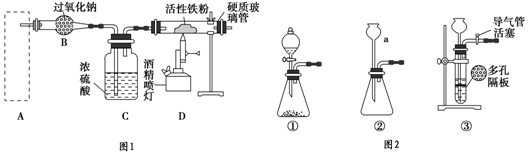
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com