
【题目】氯、磷的化合物广泛用于农药、医药、染料等领域。
(1)PCl3与氯气、水反应,得到HCl气体和一种无色透明有刺激性臭味的液体X,实验测定,1 mol的H2O完全反应会生成2 mol的HCl,则X的组成元素是______________;已知X的相对分子质量为153.5,则X的化学式为________________。
(2)X在高温与O2发生反应,形成P4O10(固态)和Cl2。将3.07 g X与448 mLO2(已折算至标准状况,下同)在高温下充分反应后,生成Cl2____mol,气体的体积将变为_____mL。
(3)白磷在氯气中燃烧,一般得到PCl3和PCl5的混合物。2.48 g白磷(P4),与一定量的氯气恰好完全反应,产物的总质量为14.55 g,计算产物中PCl3的质量分数____________(保留3小数)。
【答案】磷、氧、氯 POCl3 0.03 784 0.284
【解析】
(1)根据信息:PCl3与氯气、水反应,得到HCl气体和X,1mol的H2O完全反应会生成2mol的HCl,反应方程式应为xPCl3+H2O+yCl2=2HCl+xX,根据原子守恒知道X中含有磷、氧、氯三种元素。反应中氯气被还原,则P元素被氧化成+5价,再结合X的相对分子质量为153.5可得X的化学式为POCl3;
(2)POCl3在高温与O2发生反应,形成P4O10(固态)和Cl2,该反应中O2被还原,Cl元素被氧化,结合电子守恒和元素守恒可得方程式为:4POCl3+3O2=P4O10+6Cl2;
将3.07g即0.02molPOCl3,与448mL即0.02molO2在高温下充分反应后,POCl3全部反应,O2有剩余,生成Cl2的量按照POCl3进行计算,根据方程式可知Cl2的物质的量是0.03mol,消耗氧气是0.025mol,剩余氧气是0.005mol,气体的体积将从0.02mol变为0.005mol+0.03mol=0.035mol,体积是0.035mol×22.4L/mol=0.784L=784mL;
(3)白磷在氯气中燃烧,设得到PCl3和PCl5的物质的量分别是xmol、ymol,则x+y=![]() ×4=0.08,137.5x+208.5y=14.550,解得x=0.03mol,y=0.05mol,则三氯化磷的质量分数=
×4=0.08,137.5x+208.5y=14.550,解得x=0.03mol,y=0.05mol,则三氯化磷的质量分数=![]() ×100%=28.4%=0.284。
×100%=28.4%=0.284。


科目:高中化学 来源: 题型:
【题目】锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀―现象产生电能,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是( )
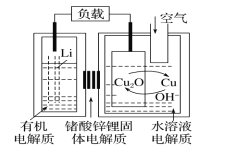
A.放电时,Li+透过固体电解质向右移动
B.放电时,正极的电极反应式为O2+2H2O+4e-=4OH-
C.通空气时,铜被腐蚀,表面产生Cu2O
D.整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
完成下列填空
(1)氮原子的电子排布式为_________,Z元素在元素周期表中的位置为______
(2)上表中原子半径最大的元素是(写元素符号) _____________,该原子的核外电子占有_____________个轨道,有___________种运动状态。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是______________
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1moY单质比1mol硫单质得电子多
c.Y和硫两元素单最低价氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1molX的高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出:X的电子式为______________该反应的热化学方程式__________________
(5)简述碳的同位素中一种原子的用途___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,0.1000 mol/L Na2CO3溶液25 mL用0.1000 mol/L盐酸滴定,其滴定曲线如图。
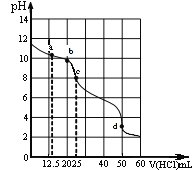
对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是
A.a点:c(CO32-)>c(HCO3-)>c(OH-)
B.b点:5c(Cl-)>4c(HCO3-)+4c(CO32-)
C.c点:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D.d点:c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萘普生是重要的消炎镇痛药。以下是它的一种合成路线:
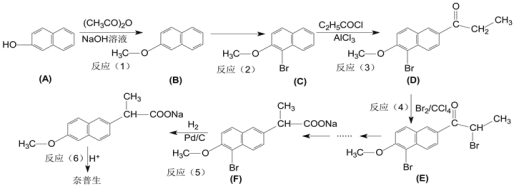
已知:萘(![]() )的化学性质与苯相似。
)的化学性质与苯相似。
(1)反应①的反应类型是_______________。萘普生的分子式是____________________。
(2)反应②的试剂和条件是___________。反应③的产物是D和_____________(填化学式)。
(3)若省略反应②和⑤,B物质与C2H5COCl反应,除生成H(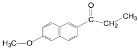 )外,最有可能生成的副产物(与H互为同分异构体)的结构简式是__________________。
)外,最有可能生成的副产物(与H互为同分异构体)的结构简式是__________________。
(4)X是D一种同分异构体,具有以下特点:
①萘的衍生物;②有两个取代基且在同一个苯环上;③在NaOH溶液中完全水解,含萘环的水解产物中有5种化学环境不同的氢。写出X可能的结构简式_____(任写一种)。
(5)根据已有知识并结合上述合成路线中的相关信息写出以苯和CH3COCl为原料制备:![]() 的合成路线流程图___________(无机试剂任用)。(合成路线流程图示例如下:CH3CHO
的合成路线流程图___________(无机试剂任用)。(合成路线流程图示例如下:CH3CHO![]() CH3CH2OH
CH3CH2OH![]() CH3CH2ONa)
CH3CH2ONa)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )
A.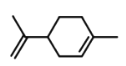 和
和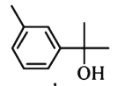 都属于芳香族化合物
都属于芳香族化合物
B. 和
和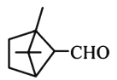 分子中所有碳原子均处于同一平面上
分子中所有碳原子均处于同一平面上
C. 、
、 和
和 均能使酸性
均能使酸性![]() 溶液褪色
溶液褪色
D. 和
和 均能与新制的
均能与新制的![]() 反应生成红色沉淀
反应生成红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )

A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是原子形成简单离子转移的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组表述中,两个原子不属于同种元素原子的是( )
A.3p能级有一个空轨道的基态原子和核外电子的排布式为1s22s22p63s23p2的原子
B.2p能级无空轨道,且有一个未成对电子的基态原子和原子的最外层电子排布式为2s22p5的原子
C.M层全充满而N层为4s2的原子和核外电子排布式为1s22s22p63s23p64s2的原子
D.最外层电子数是核外电子总数1/5的原子和最外层电子排布式为4s24p5的原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素A、B、C、D、E原子序数依次增大。已知:A、C同主族,A的原子最外层电子数是次外层的3倍,B的氧化物既能溶于强酸,又能溶于强碱,D的原子半径是第3周期中最小的,E是形成骨骼和牙齿的主要元素,且E单质能和水反应。则下列分析错误的是
A. A的离子结构示意图为![]()
B. D的最高价氧化物的水化物的酸性大于C的最高价氧化物的水化物的酸性
C. E和D形成的离子化合物ED2的电子式为![]()
D. B的氧化物为离子化合物,只含离子键,其晶体为离子晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com