
 实验室需要0.1mol/L NaOH溶液450mL,需要0.5mol/L硫酸溶液500mL.根据这两种溶液的配置情况回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL,需要0.5mol/L硫酸溶液500mL.根据这两种溶液的配置情况回答下列问题:分析 (1)根据各仪器的作用选取仪器;
(2)由于实验室无450mL容量瓶,故应选用500mL容量瓶,配制出500mL溶液,根据质量m=CVM来计算;
(3)根据“大而近”的原则,根据需要量取的浓硫酸的体积来选择合适的量筒;
(4)根据各物理量的多少与体积是否有关判断.
(5)根据c=$\frac{n}{V}$分析操作对溶质的物质的量或对溶液的体积的影响判断.
解答 解:(1)用容量瓶配制溶液,用胶头滴管定容;还需要用到的仪器有:溶解或稀释药品的烧杯、搅拌或引流用的玻璃棒,
故答案为:AC;烧杯和玻璃棒;
(2)由于实验室无450mL容量瓶,故应选用500mL容量瓶,配制出500mL溶液,故所需的氢氧化钠的质量m=CVM=0.1mol/L×0.5L×40g/mol=2.0g,故答案为:2.0;
(3)根据“大而近”的原则,根据需要量取的浓硫酸的体积为13.6mL可知应选择15mL的量筒,故答案为:15;
(4)A.溶液中H2SO4的物质的量n=CV,所以与溶液的体积有关,故错误.
B.溶液的浓度c=$\frac{1000ρω}{M}$,与所量取的体积无关,故正确.
C.溶液中SO42-的数目N=CVNA,所以与溶液的体积有关,故错误.
D.溶液的密度与所量取溶液的体积无关,故正确.
故选:BD;
(5)A.烧杯未进行洗涤,会导致溶质的损失,则浓度偏低,故A错误;
B.配置前,容量瓶中有少量蒸馏水,对溶液浓度无影响,故B错误;
C.在容量瓶中定容时俯视容量瓶刻度线,则溶液体积偏小,故浓度偏高,故C正确;
D.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线是正常的,再加水至刻度线会导致浓度偏低,故D错误.
故选C.
点评 本题考查了一定物质的量浓度溶液的配制,难度不大,易错题是(2)题,注意需要450mL溶液,因为没有450mL的容量瓶,有500mL的容量瓶,所以要配制500mL溶液,所称量固体的质量或量取溶液的体积应等于配制500mL溶液时所用的量.


科目:高中化学 来源: 题型:选择题
| A. | 肯定含有SO2和NO | B. | 肯定含有NO和O2 | ||
| C. | 可能有Cl2 | D. | 肯定没有Cl2、NO2,可能有O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Fe2+、Na+、Ba2+、Al3+ |
| 阴离子 | Cl-、SO42-、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 125.0克CuSO4•5H2O 晶体 | B. | 76.8克无水CuSO4 固体 | ||
| C. | 120.0克CuSO4•5H2O 晶体 | D. | 40.0克无水CuSO4固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取无水MgCl2,将MgCl2溶液直接蒸干 | |
| B. | 除去CuCl2溶液中含有的少量FeCl2,向溶液中加入过量CuO,待充分反应后过滤 | |
| C. | 的检验:取少量试样于试管中,滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,则试样中含有 | |
| D. | 探究反应的限度:将1mL0.1mol•L-1的KI溶液与5mL0.1mol•L-1的FeCl2溶液混合,待充分反应后,滴加KSCN溶液,观察实验现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氟原子的结构示意图: | B. | 塑料王聚四氟乙烯的结构简式: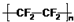 | ||
| C. | 中子数为10的氟原子:${\;}_{9}^{19}$F | D. | 萤石主要成分CaF2电子式: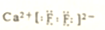 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
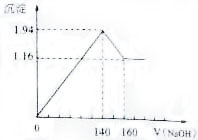 将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为0.5 mol/L的NaOH溶液,生成的沉淀质量跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)求:(1)合金中Mg,Al的质量;
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为0.5 mol/L的NaOH溶液,生成的沉淀质量跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)求:(1)合金中Mg,Al的质量;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com