

���� ��1������26��Ԫ�أ���ԭ�Ӻ�����26�����ӣ���ԭ��ʧȥ2�����ӱ���������ӣ����ݹ���ԭ��д���������Ӻ�������Ų�ʽ��
��2������N��Oԭ�Ӽ۲���Ӷ������ж��ӻ���ʽ��NH2OH�д���������е�ϸߣ�
��3���ɽṹ��֪��Fe2+��6��Nԭ��֮���γ���λ����
��4������Clԭ�Ӽ۲���Ӷ������¶Ե��������жϿռ�ṹ��
��5�����þ�̯��ȷ���仯ѧʽ��
��� �⣺��1������26��Ԫ�أ���ԭ�Ӻ�����26�����ӣ���ԭ��ʧȥ2�����ӱ���������ӣ�Fe2+�ڻ�̬ʱ��������Ų�ʽΪls22s22p63s23p63d6��
�ʴ�Ϊ��ls22s22p63s23p63d6��
��2���ǰ������У��۲���Ӷ�Ϊ4��ԭ����N��Oԭ�ӣ����Բ���sp3�ӻ���ԭ����N��Oԭ�ӣ�NH2OH����֮�����������е�ϸߣ�
�ʴ�Ϊ��N��O��NH2OH����֮����������
��3���ɽṹ��֪��Fe2+��6��Nԭ��֮���γ���λ��������λ��Ϊ6���ʴ�Ϊ��6��
��4��ClO4-����Clԭ�Ӽ۲���Ӷ���Ϊ4+$\frac{7+1-2��4}{2}$=4��û�й¶Ե��ӣ���ռ�ṹΪ�������壬�ʴ�Ϊ���������壻
��5����ԭ�Ӹ���=8��$\frac{1}{8}$����ԭ�Ӹ�����1�������仯ѧʽΪFe4N���ʴ�Ϊ��Fe4N��
���� �����漰��ѧʽ��ȷ������λ�����жϡ��ӻ���ʽ���жϵ�֪ʶ�㣬��Щ���ǿ����ȵ㣬�ѵ�����λ����ȷ�������ݸ�����ȷ�����ɣ��Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/s | ��0 | ��50 | ��150 | ��250 | ��350 |
| ��n��PCl3��mol | ��0 | ��0.16 | ��0.19 | ��0.20 | ��0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
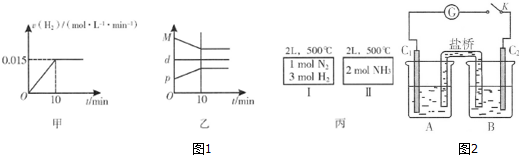
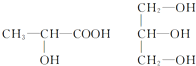 ��Ҫ������������⣮
��Ҫ������������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ������ | B�� | ����Ԫ�� | C�� | ����Ԫ�� | D�� | ±��Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��֪NH3��HCl������������Ȫʵ������壬����ͬ��ͬѹ���õ������ƿһ���ռ���NH3����һ���ռ�HCl��N2�Ļ�����壬��ͼ��ʾ����Ȫʵ��ֹͣ��������ƿ����Һ�����ʵ����ʵ���Ũ�ȣ�c�������ʵ�����������w����ϵ�ǣ�������
��֪NH3��HCl������������Ȫʵ������壬����ͬ��ͬѹ���õ������ƿһ���ռ���NH3����һ���ռ�HCl��N2�Ļ�����壬��ͼ��ʾ����Ȫʵ��ֹͣ��������ƿ����Һ�����ʵ����ʵ���Ũ�ȣ�c�������ʵ�����������w����ϵ�ǣ�������| A�� | c��w����ͬ | B�� | c��w����ͬ | C�� | c��ͬ��w��ͬ | D�� | w��ͬ��c��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ�ͺ�ֲ���Ͷ��ǻ��������ڲ�ͬ����л��� | |
| B�� | ������������������ƣ������ܱ����Ը��������Һ���� | |
| C�� | ������K2Cr2O7 ��Һ�����Ҵ�����ȩ��Һ | |
| D�� | ��ά�ء����ǡ������Ǻ͵���ø��һ�������¶��ɷ���ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڻ�ѧ��Ӧ�����У��������ʱ仯��ͬʱ��һ�����������仯 | |
| B�� | ��101 kPaʱ��2 g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ���������ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ2H2 ��g��+O2 ��g���T2H2O��l����H=-571.6 kJ/mol | |
| C�� | �����ǡ����ȫ��Ӧ�������ε�c��H+��=c��OH-��=10-6 mol/L����Һһ�������� | |
| D�� | �¶ȡ�Ũ�ȵĸı�һ��������Ӧ���ʵĸı䣬���Ի�ѧƽ��һ�����ƶ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com