
| A. | 同周期元素的原子半径以ⅦA族的最大 | |
| B. | 同主族两种元素原子的核外电子数的差值可能为36 | |
| C. | 短周期中次外层电子数是最外层电子数2倍的原子一定是非金属元素的原子 | |
| D. | 科学家在周期表中金属与非金属分界线处找到了优良的催化剂 |
分析 A.同周期元素中原子半径从左向右逐渐减小;
B.根据核外电子排布判断;同主族相间两种元素的核外电子数相差可能为36;
C.短周期元素中次外层电子数是最外层电子数2倍的元素的有Li、Si等元素;
D.在周期表中金属与非金属分界线常作半导体.
解答 解:A.因同周期元素中原子半径从左向右逐渐减小,则同周期元素中ⅦA族元素的原子半径最小,故A错误;
B.原子的原子序数等于核外电子数,每周期中含有的元素种类数分别为:2、8、8、18、18、32种元素,因此同主族相间的两种元素之间原子序数相差36存在,故B正确;
C.短周期元素中次外层电子数是最外层电子数2倍的元素的有Li、Si两种元素,Li金属,故C错误;
D.在金属和非金属的分界线处元素的单质的导电性介于导体与绝缘体之间,属于半导体,所以在周期表中金属与非金属分界线处找到的是半导体,故D错误.
故选B.
点评 本题考查了同周期元素原子半径大小、同主族元素原子序数关系、最外层核外电子数和此外层电子数的关系,判断元素的种类、以及元素周期律的应用等知识点.


科目:高中化学 来源: 题型:填空题
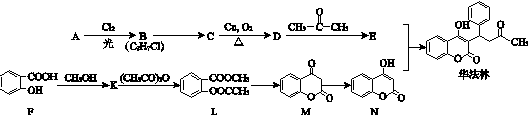
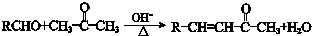
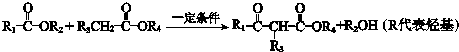
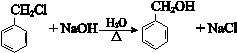 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A到F是原子序数依次增大的前四周期元素:
A到F是原子序数依次增大的前四周期元素:| A | A是原子半径最小的元素 |
| B | B基态原子的价层电子排布式为nsnnpn |
| D | D原子最外层电子数是次外层电子数的三倍 |
| E | C的三价阴离子和E的二价阳离子具有相同的电子层结构 |
| F | F元素的基态原子有六个成单电子 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是周期表中原子序数小于20的9种元素单质的沸点与原子序数的关系,图中原子序数是连续的.试根据如图,回答下列问题:
如图是周期表中原子序数小于20的9种元素单质的沸点与原子序数的关系,图中原子序数是连续的.试根据如图,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉漂白物质时发生的发应和变质失效时的反应一样 | |
| B. | 将氯气溶于水中,当水中各成分浓度保持不变时,即表示反应停止 | |
| C. | 二氧化硅固体是由原子直接构成的,那么固态二氧化碳也是由原子直接构成 | |
| D. | 碱金属(如钾、钠等)可以存放在所有有机溶剂中,而白磷则应保存在水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 应称取氢氧化钠固体的质量/g | 应选用容量瓶的规格/mL | 除烧杯、托盘天平、容量瓶、量筒外还需的其它仪器 |
| 10.0 | 250 | 玻璃棒、胶头滴管、药匙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com