
【题目】有机化合物M是一种药品辅料的中间体,下图是该有机化合物的合成线路。请回答下列问题。
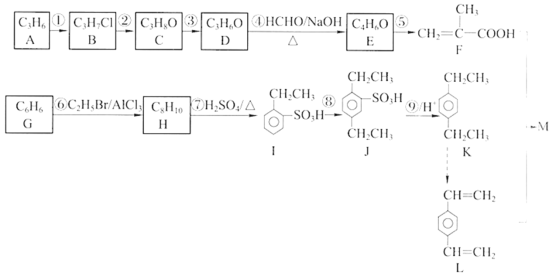
已知: i.
ii.两种或两种以上的单体发生的加聚反应称为共聚反应,如:

(1)A的结构简式是_________。
(2)反应②的化学方程式是_________。
(3)合成线路①~⑤中属于氧化反应的有_________(填序号)。
(4)反应④的化学方程式是_________。
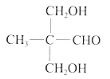
(5)若1mol D与2mol HCHO反应,该反应产物的结构简式是_________。
(6)反应⑧的反应物及反应条件是_________。
(7)合成线路中⑦~⑨的目的是_________。
(8)在一定条件下,F与L按物质的量之比1 : 1发生共聚反应合成M,其链节中不含碳碳双键,且除苯环外不含其他环状结构,则M的结构简式是_________。
【答案】CH3CH=CH2 CH3CH2CH2Cl+NaOH![]() CH3CH2CH2OH+NaCl ③⑤
CH3CH2CH2OH+NaCl ③⑤ 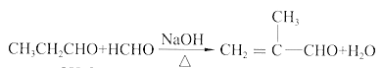
 反应物是C2H5Br, 用AlCl3作催化剂 利用—SO3H 基团,占据乙苯的邻位,使反应⑧中乙基主要在乙苯的对位取代,以减少副反应的发生
反应物是C2H5Br, 用AlCl3作催化剂 利用—SO3H 基团,占据乙苯的邻位,使反应⑧中乙基主要在乙苯的对位取代,以减少副反应的发生 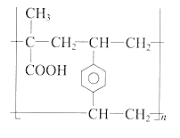
【解析】
结合E的分子式和F的结构简式可知,E氧化生成F,推知E为![]() ,D与甲醛在氢氧化钠中加热发生类似已知: i.
,D与甲醛在氢氧化钠中加热发生类似已知: i.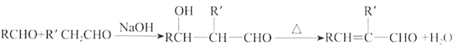 的反应,得到E,可推知D为CH3CH2CHO,C为CH3CH2CH2OH,B为CH3CH2CH2Cl,则A为CH3CH=CH2;苯与溴乙烷在氯化铝作用下发生反应生成乙苯H,乙苯与浓硫酸发生磺化反应生成I为邻乙基苯磺酸,邻乙基苯磺酸溴乙烷在氯化铝作用下发生反应生成J为
的反应,得到E,可推知D为CH3CH2CHO,C为CH3CH2CH2OH,B为CH3CH2CH2Cl,则A为CH3CH=CH2;苯与溴乙烷在氯化铝作用下发生反应生成乙苯H,乙苯与浓硫酸发生磺化反应生成I为邻乙基苯磺酸,邻乙基苯磺酸溴乙烷在氯化铝作用下发生反应生成J为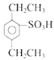 ,
, 酸化得到K为
酸化得到K为![]() ,
,![]() 在一定条件下发生一系列反应得到L为
在一定条件下发生一系列反应得到L为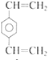 ,
, 与
与![]() 反应生成M为
反应生成M为 ,据此分析解答。
,据此分析解答。
(1)根据以上分析,A的结构简式是CH3CH=CH2;
(2)反应②是CH3CH2CH2Cl在氢氧化钠的水溶液中加热发生水解反应生成CH3CH2CH2OH和氯化钠,反应的化学方程式是CH3CH2CH2Cl+NaOH![]() CH3CH2CH2OH+NaCl;
CH3CH2CH2OH+NaCl;
(3)合成线路①~⑤中属于氧化反应的有③⑤;
(4)反应④是丙醛和甲醛在氢氧化钠中加热发生反应生成![]() 和水,反应的化学方程式是
和水,反应的化学方程式是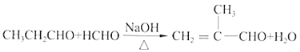 ;
;
(5)若1mol D(CH3CH2CHO)与2mol HCHO反应,丙醛中醛基相连的碳上两个碳氢键断裂加成在甲醛上,该反应产物的结构简式是 ;
;
(6)反应⑧与反应⑥相似,邻乙基苯磺酸溴乙烷在氯化铝作用下发生反应生成J,反应物是C2H5Br,用AlCl3作催化剂;
(7)合成线路中⑦~⑨的目的是利用—SO3H 基团,占据乙苯的邻位,使反应⑧中乙基主要在乙苯的对位取代,以减少副反应的发生;
(8)在一定条件下,F(![]() )与L(
)与L( )按物质的量之比1 : 1发生共聚反应合成M,其链节中不含碳碳双键,且除苯环外不含其他环状结构,则M的结构简式是
)按物质的量之比1 : 1发生共聚反应合成M,其链节中不含碳碳双键,且除苯环外不含其他环状结构,则M的结构简式是 。
。


科目:高中化学 来源: 题型:
【题目】辉铜矿石主要含有硫化亚铜(Cu2S),还含有FeO、CaO、SiO2等。以辉铜矿石为原料制备CuCl2·2H2O的工艺流程如图所示:
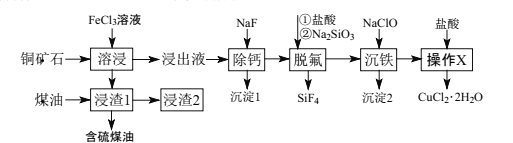
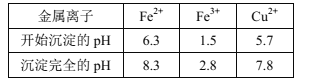
已知:Ⅰ.金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
Ⅱ.NaCl易溶于水,不溶于酒精,随温度变化溶解度变化不明显;CuCl2·H2O易溶于水,酒精,浓氨水,随温度升高溶解度变化明显增大。
Ⅲ.Ksp(CaF2)=4.0×10-11
(1)为了提高“溶浸”效率,可采取的措施是___。写出“溶浸”过程中Cu2S溶解时离子方程式:___。
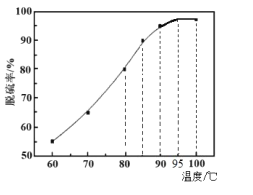
(2)“脱硫”时,随着温度的升高,脱硫率呈上升趋势(如图),原因是___。
(3)写出“脱氟”时HF发生反应的化学方程式:___。
(4)“沉铁”过程中,加入NaClO的两个作用是___。
(5)“操作X”的具体操作是___。
(6)经过“操作X”后,母液经过一系列操作可得到另外一种物质,要得到这种纯净物,最好选用下列试剂洗涤___。
A.浓盐酸 B.水 C.酒精 D.浓氨水
(7)向“浸出液”中加入NaF除去溶液中Ca2+(浓度为1.0×10-3mol·L-1),当溶液中c(F-)=2.0×10-3mol·L-1时,除钙率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某抗结肠炎药物的有效成分的合成路线如图所示(部分试剂和反应条件已略去):
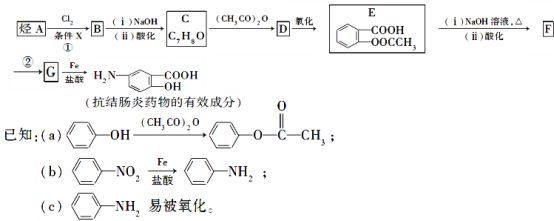
请回答下列问题:
(1)E中含有的官能团为__。
(2)②的反应类型是__。
(3)下列对抗结肠炎药物的有效成分可能具有的性质推测不正确的是__(填字母)。
a.水溶性比苯酚的好,密度比苯酚的大
b.能发生消去反应
c.能发生加聚反应
d.既有酸性又有碱性
(4)①的反应方程式为__。
(5)符合下列条件的E的同分异构体有__种。写出其中核磁共振氢谱中有四组峰的结构简式:__。
a.与E具有相同的官能团且官能团不在同一侧链上
b.水解产物之一能与氯化铁溶液发生显色反应
(6)连有烷基的苯环上再引入一个取代基时,常取代烷基邻、对位上的氢原子,而连有羧基的苯环上再引入一个取代基时,常取代羧基间位上的氢原子。据此设计出以A为原料合成![]() 的路线(仿照题中抗结肠炎药物的有效成分的合成路线进行答题)___。
的路线(仿照题中抗结肠炎药物的有效成分的合成路线进行答题)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用电化学方法处理石油炼制过程中产生的含H2S的废气。基本工艺是将H2S通入FeCl3溶液中,过滤后将滤液加入电解槽中电解,电解后的滤液可以循环利用。下列有关说法正确的是( )
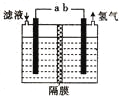
A.过滤得到的沉淀可能是FeS
B.与a极相连的电极反应式为Fe2+- e-= Fe3+
C.可以用Fe与外接电源a极相连
D.若有0.10mol电子转移,则一定能得到1.12L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国药物学家最近合成一种可能用于治疗高血压的有机物K,合成路线如下:
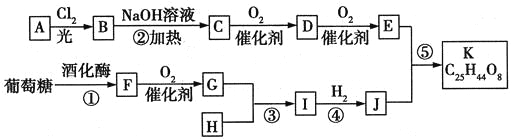
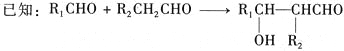
其中A属于碳氢化合物,其中碳的质量分数约为83.3%;E的核磁共振氢谱中只有2组吸收峰。H常温下呈气态,是室内装潢产生的主要污染物之一。G和H以1:3反应生成I。
试回答下列问题:
(1)A的分子式为:______________。
(2)写出下列物质的结构简式:D:____________;G:___________。
(3)反应①―⑤中属于取代反应的有___________。
(4)反应①的化学方程式为_______________;反应④的化学方程式为_________________。
(5)E有多种同分异构体,符合“既能发生银镜反应又能发生水解反应”条件的E的同分异构体有_______种,写出符合上述条件且核磁共振氢谱只有2组吸收峰的E的同分异构体的结构简式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 的原子序数依次增大。
的原子序数依次增大。![]() 与
与![]() 同周期且相邻,
同周期且相邻,![]() 的基态原子的
的基态原子的![]() 电子数与
电子数与![]() 电子数相等,乙是地壳中含量最多的金属元素,
电子数相等,乙是地壳中含量最多的金属元素,![]() 的原子核外价电子排布式为
的原子核外价电子排布式为![]() ,
,![]() 的基态原子的未成对电子数是同周期元素中最多的。下列说法错误的是( )
的基态原子的未成对电子数是同周期元素中最多的。下列说法错误的是( )
A.简单气态氢化物的稳定性:![]()
B.简单离子的半径:![]()
C.![]() 的最高价氧化物对应的水化物既能与强酸反应,又能与强碱反应
的最高价氧化物对应的水化物既能与强酸反应,又能与强碱反应
D.由![]() 、
、![]() 、
、![]() 三种元素形成的某种化合物可用于检查司机是否酒后驾车
三种元素形成的某种化合物可用于检查司机是否酒后驾车
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酸酯类物质广泛用于建筑、包装材料等,丙烯酸是合成丙烯酸酯的原料之一。丙烯醇可用于生产甘油、塑料等。以丙烯醛为原料生产丙烯醇、丙烯酸的流程如图所示:

已知:
①2CH2=CH-CHO+NaOH![]() CH2=CHCH2OH+CH2=CHCOONa
CH2=CHCH2OH+CH2=CHCOONa
②2CH2=CHOONa+H2SO4→2CH2=CHCOOH+Na2SO4
③有关物质的相关性质如表:
物质 | 丙烯醛 | 丙烯醇 | 丙烯酸 | 四氯化碳 |
沸点/℃ | 53 | 97 | 141 | 77 |
熔点/℃ | - 87 | - 129 | 13 | -22.8 |
密度/g·mL-3 | 0.84 | 0.85 | 1.02 | 1.58 |
溶解性(常温) | 易溶于水和有机溶剂 | 溶于水和有机溶剂 | 溶于水和有机溶剂 | 难溶于水 |
(1)操作①需要连续加热30min,所用装置如图所示。仪器L名称是________。

(2)操作②使用的主要仪器是分液漏斗,在使用之前需进行的操作是 ___。
(3)操作④包括____、过滤、冰水洗涤、低温吸干。
(4)操作⑤中,加热蒸馏“下层液体”,分离出四氯化碳;再分离出丙烯醇(如图),要得到丙烯醇应收集 ____(填温度)的馏分。图中有一处明显错误,应改为____。

(5)测定丙烯醇的摩尔质量:准确量取amL丙烯醇于分液漏斗中,烧瓶内盛装足量钠粒。实验前量气管B中读数为b mL,当丙烯醇完全反应后,冷却至室温、调平B、C液面,量气管B的读数为c mL。已知室温下气体摩尔体积为VL·mol-1。

调平B、C液面的操作是____;实验测得丙烯醇的摩尔质量为____g·mol-1(用代数式表示)。如果读数时C管液面高于B管,测得结果将____(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铝(AlPO4)是一种用途广泛的材料,在建筑、耐火材料、化工等方面具有广泛的应用前景。以磷硅渣(主要成分为Ca3(PO4)2、Al2O3、SiO2和V2O5等)为原料制备磷酸铝的工艺流程如图所示:

回答下列问题:
(1)酸浸液中含磷元素的主要粒子是_____(填化学式,下同),浸渣中的主要化学成分是_____。
(2)生石灰除了调节pH外,另一作用是_____。
(3)滤液中钒元素以V3O93-形式存在,V3O93-易水解为[VO3(OH)]2-,该水解反应的离子方程式为_____。
(4)碱浸时,粗磷酸铝转化为可溶性溶质,则可溶性溶质分别是_____ (填化学式)。
(5)实验测得pH、反应温度与时间对碱浸时固相中P、Al含量的影响如图所示:

则最优反应条件是_____。
(6)固相反应制备磷酸铝的方法之一是在900℃的焙烧炉内加热磷酸二氢铵与氧化铝混合物,写出该反应的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO3溶液的浓度,现用0.2000mol/L的酸性KMnO4溶液进行滴定,回答下列问题:
(1) 配平离子方程式:______MnO4-+HSO3-+H+=Mn2++SO42-+H2O。
(2)用KMnO4进行滴定时,KMnO4溶液应装在_______________中,判断滴定终点的现象是_______。
(3)下列操作会导致测定结果偏高的是_________。
A. 盛装未知浓液的锥形瓶用蒸馏水洗过,未用待测液润洗
B. 未用标准浓度的酸性KMnO4溶液润洗滴定管
C. 观察读数时,滴定前仰视,滴定后俯视
D. 滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
(4) 根据下表测定的实验数据,计算KMnO4溶液体积的平均值为___mL;NaHSO3溶液的物质的量浓度为___mol/L(数据精确到0.1)。
试验编号 | 待测NaHSO3溶液的体积/ mL | KMnO4溶液体积/ mL |
1 | 20.00 | 15.98 |
2 | 20.00 | 17.00 |
3 | 20.00 | 16.02 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com