
分析 根据化合价变化可知Zn被氧化,应为原电池的负极,电极反应为Zn+2OH-=Zn(OH)2+2e-,则正极为Ag2O,被还原,电极反应为Ag2O+H2O+2e-=2Ag+2OH-,结合电极方程式解答该题.
解答 解:(1)在反应Ag2O+Zn+H2O═2Ag+Zn(OH)2中,由化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,电子由负极流向正极,电流流向与电子流向相反,故答案为:Ag2O;Zn
(2)正极发生还原反应,负极的电极反应式为:Zn+2OH-=Zn(OH)2+2e-,故答案为:还原;Zn+2OH-=Zn(OH)2+2e-;
(3)阴离子向负极移动,正极的电极反应式为:Ag2O+H2O+2e-=2Ag+2OH-,导致正极附近氢氧根离子浓度增大,溶液的pH值增大,故答案为:Zn;增大.
点评 本题考查原电池知识,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意根据电极反应判断原电池的正负极以及电池反应.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
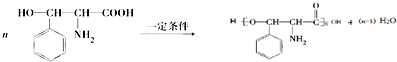 .
.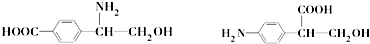
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
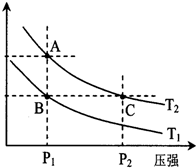 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)△H<0
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)△H<0查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中的能量变化都表现为热量的变化 | |
| B. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 | |
| C. | 反应物的总能量低于生成物的总能量时,发生吸热反应 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 FeCl3溶液可用作印刷电路铜板的腐蚀剂,该腐蚀过程的离子方程式为2Fe3++Cu=2Fe2++Cu2+.若将该反应设计成原电池,请在如图方框中画出原电池的装置简图,标出正、负极及两极材料和电解质溶液.
FeCl3溶液可用作印刷电路铜板的腐蚀剂,该腐蚀过程的离子方程式为2Fe3++Cu=2Fe2++Cu2+.若将该反应设计成原电池,请在如图方框中画出原电池的装置简图,标出正、负极及两极材料和电解质溶液.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x+y=5 | B. | x+y=7 | C. | x+y=11 | D. | x+y=13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3 | B. | FeCl2 | C. | Na2O2 | D. | NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com