
����Ŀ����֪XΪһ�ֳ������Ũ��Һ����ʹ���DZ�ڡ�A��X��Ӧ��ת����ϵ��ͼ��ʾ�����з�Ӧ���������ֲ��������ȥ���������й�˵����ȷ����
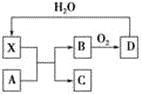
A. Xʹ���DZ�ڵ�������Ҫ������X����ˮ��
B. ��AΪ����������A��X�������¼�����ȫ��Ӧ
C. ��AΪ̼���ʣ���Cͨ�������ij���ʯ��ˮ�У�һ�����Թ۲쵽��ɫ��������
D. ��ҵ�ϣ�Bת��ΪD�ķ�Ӧ����Ϊ���¡���ѹ��ʹ�ô���
���𰸡�A
��������XΪһ�ֳ������Ũ��Һ����ʹ���Ƿ�ĩ��ڣ���X�����ᣬD��ˮ��Ӧ�������ᣬ��D����������B��������Ӧ��������������B�Ƕ�������A��Xʹ���DZ�ڵ�������Ҫ������XŨ�������ˮ�ԣ���A��ȷ��B����A�����������£�����Ũ���ᷢ���ۻ�����������������ȫ�ܽ⣬��B����C����A��̼��Ũ�����̼��Ӧ���ɶ�����̼�����������ˮ��������̼�������������Ʒ�Ӧ���ɿ����Ե�̼����ƣ���C����D����ҵ�ϣ���������ת��Ϊ��������ķ�Ӧ����Ϊ���¡���ѹ��ʹ�ô�������D��ȷ����ѡAD��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ2L���ܱ������г���һ������H2O��CO��ά��700�淢����Ӧ��CO(g) + H2O(g)![]() CO2(g) + H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�(����t1<t2)��
CO2(g) + H2(g)����Ӧ�����вⶨ�IJ������ݼ��±�(����t1<t2)��
��Ӧʱ��/min | n(CO)/mol | H2O/ mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
����˵����ȷ����
A. ��Ӧ��t1 min�ڵ�ƽ������Ϊv(H2)��0.40/t1 mol��L��1��min��1
B. �����������䣬��ʼʱ�����г���0.60molCO��1.20 molH2O����ƽ��ʱ��n(CO2)��0.40 mol
C. ���������������䣬��ƽ����ϵ����ͨ��0.20 molH2O����ԭƽ����ȣ��ﵽ��ƽ��ʱCOת��������H2O�����������С
D. ���¶�����800�棬������Ӧ��ƽ�ⳣ��Ϊ0.64��������ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ӦN2��3H2![]() 2NH3�������仯��ͼ��ʾ���÷�Ӧ���Ȼ�ѧ����ʽ��( )
2NH3�������仯��ͼ��ʾ���÷�Ӧ���Ȼ�ѧ����ʽ��( )
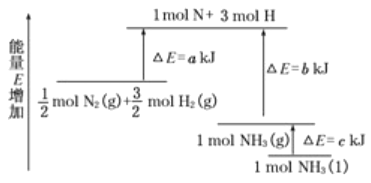
A. N2(g)��3H2(g) ![]() 2 NH3(l) ��H��(b��c��a) kJ��mol��1
2 NH3(l) ��H��(b��c��a) kJ��mol��1
B. N2(g)��3H2(g) ![]() 2NH3(g) ��H��(a��b) kJ��mol��1
2NH3(g) ��H��(a��b) kJ��mol��1
C. N2(g)��3H2(g) ![]() 2NH3(l) ��H��2(a��b��c) kJ��mol��1
2NH3(l) ��H��2(a��b��c) kJ��mol��1
D. N2(g)��3H2(g) ![]() 2NH3(g) ��H��2(b��a) kJ��mol��1
2NH3(g) ��H��2(b��a) kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б����в���ȷ����( )
A. 1 mol�� B. 1 mol H C. 1 mol SO42�� D. 1 mol CH4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼���ã����ܼ��š��ǵ������羭�÷�չ����˼·��������Ϊ��֮�������
A. �������ܡ�̫���ܵ�����Դ
B. ���մ�����ҵ����
C. ������չ����Դ����
D. ���ȿ���ú��ʯ�ͺ���Ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϡ�����ϡ����Ļ����Һ200 mL��ƽ���ֳ����ݡ�������һ��������ͭ�ۣ�������ܽ�9.6 g������һ�����������ۣ�������������������������ӵı仯����ͼ��ʾ(��֪����ֻ����ԭΪNO����)�����з��������������
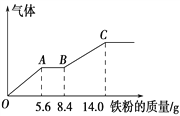
A. ԭ�������HNO3�����ʵ���Ϊ0.1 mol
B. OA�β�������NO��AB�εķ�ӦΪFe��2Fe3�� == 3Fe2����BC�β�������
C. �ڶ�����Һ����������ΪFeSO4
D. H2SO4Ũ��Ϊ2.5 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NO2��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1��NO2����ˮ���գ���Ӧ�Ļ�ѧ��Ӧ����ʽΪ__________________________________��
���÷�Ӧ6NO2��8NH3![]() 7N2��12 H2OҲ�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������______________ L
7N2��12 H2OҲ�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������______________ L
��2����֪��2SO2��g��+O2��g��![]() 2SO3��g�� ��H=-196.6 kJ��mol-1
2SO3��g�� ��H=-196.6 kJ��mol-1
2NO��g��+O2��g��![]() 2NO2��g�� ��������H=-113.0 kJ��mol-1
2NO2��g�� ��������H=-113.0 kJ��mol-1
��ӦNO2��g��+SO2��g��![]() SO3��g��+NO��g������H=________kJ��mol-1��һ�������£���NO2��SO2�������1:2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����________��
SO3��g��+NO��g������H=________kJ��mol-1��һ�������£���NO2��SO2�������1:2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����________��
a.��ϵѹǿ���ֲ��� �������������� b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ��䡡��������d��ÿ����1 mol SO3��ͬʱ����1 molNO2
���������Ӧƽ��ʱNO2��SO2�����Ϊ1:6����ƽ�ⳣ��K��__________��
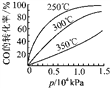
��3��CO�����ںϳɼ״�����Ӧ����ʽΪCO��g��+2H2��g��![]() CH3OH��g����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ����ͼ��ʾ���÷�Ӧ��H______0������>������ <������ʵ����������������250�桢1.3��104kPa���ң�ѡ���ѹǿ��������________________��
CH3OH��g����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ����ͼ��ʾ���÷�Ӧ��H______0������>������ <������ʵ����������������250�桢1.3��104kPa���ң�ѡ���ѹǿ��������________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���������������ʵ���Һʱ����������ɫƿ����(����)
��Ũ���ᡡ��Ũ���ᡡ��Ũ���ᡡ����������Һ
A. �٢� B. �ڢ� C. �٢� D. �ڢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com