
| A.NO和O2+ | B.CO和NO | C.NO2和CO2 | D.SO2和ClO2 |
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.元素的非金属性:X>Y>Z |
| B.阴离子的还原性:X<Y<Z |
| C.气态氢化物的稳定性:X>Y>Z |
| D.最高价氧化物的水化物的酸性:Z>Y>X |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
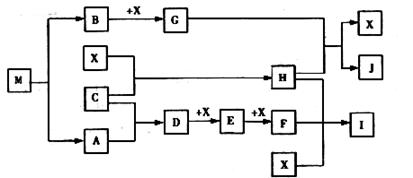
 ①写出D与X反应的化学方程式
①写出D与X反应的化学方程式 ②写出G与H反应的离子方程式。
②写出G与H反应的离子方程式。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

|
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.OH一、F—、O2—、Ne | B.CH4、NH3、H2O、HF |
| C.NH4+、Na+、H3O+、PH4+ | D.F一、O2一、Mg2+、A13+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 ,b与c形成化合物的电子式为:
,b与c形成化合物的电子式为: ,下列比较中正确的是( )
,下列比较中正确的是( )| A.原子半径a>c>b | B.原子的氧化性a>c>d |
| C.最高价氧化物的熔点a>d>b | D.最高价含氧酸的酸性c>d>a |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 甲 | 乙 | 丙 | | |
| | 丁 | 戊 | ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 水反应的化
水反应的化 学方程式为 。
学方程式为 。 式 。
式 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com