
【题目】表格中的各种情况,可以用如图的曲线表示的是( )
反 应 | 纵坐标 | 甲 | 乙 | |
A | 相同质量的氨,在同一容器中 | 氨气的转化率 | 500℃ | 400℃ |
B | 等质量钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
C | 向温度和压强都相同的甲乙两容器中分别投入体积比1:3的N2、H2(N2+3H2═2NH3) | 氨气的物质的量 | 反应过程中保持恒温恒容 | 反 应过程中保持恒温恒压 |
D | 2molSO2和1molO2 , 在相同温度下 | SO3 的浓度 | 2个大气压 | 10个大气压 |
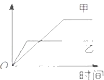
A.A
B.B
C.C
D.D
【答案】B
【解析】解:A、对于反应2NH3N2+3H2 , 温度越高化学发应速率越快,所以甲达到化学平衡用的时间短,故A错误; B、根据金属钾和金属钠与水反应的原理方程式可知,2Na~H2 , 2K~H2 , 等质量钾、钠,则金属钠的物质的量大,所以金属钠产生的氢气多,金属钾的活泼性强与金属钠,所以金属钾的反应速率快,故B正确;
C、恒温恒容就是在恒温恒压的条件下减小压强,减小压强平衡逆向移动,达平衡的时间增大,而不是缩短,故C错误;
D、对于反应2SO2+O22SO3 , 增大压强化学平衡向着正反应方向进行,所以达到平衡时,乙的三氧化硫的量高于甲的,故D错误.
故选B.
【考点精析】利用化学平衡状态本质及特征对题目进行判断即可得到答案,需要熟知化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列有关氯及其化合物的说法不正确的是
A. 工业上以氯气和澄清石灰水为原料制造漂白粉
B. 氢气在氯气中燃烧,火焰呈苍白色
C. 光照新制氯水有气泡逸出,该气体是氧气
D. 次氯酸能使染料等有机色素褪色,有漂白性,还能杀死水中的细菌,起消毒作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如图: 
回答下列问题:
(1)写H2O2的作用是并写出该步骤中发生的主要反应的离子方程式;
(2)如何检验中和反应后滤渣中阳离子已完全除尽?;
(3)写出工业制备金属铝的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某烃A的产量是衡量一个国家石油化工水平的标志,能发生下列转化关系(部分反应物或生成物及反应条件已略去):
请回答下列问题:
(1)写出下列物质的结构简式:B , D;
(2)写出下列反应A→B的化学方程式 , 反应类型;
(3)写出下列反应C+E→F的化学方程式 , 反应类型 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三种常见治疗胃病药品的标签:( )
药品中所含的物质均能中和胃里过量的盐酸,下列关于三种药片中和胃酸的能力比较,正确的是( 相对原子质量 Ca -40 C-12 O-16 H-1 Mg-24 )
A.①=②=③
B.①>②>③
C.③>②>①
D.②>③>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mLpH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中 ![]() 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mLpH=11的NaOH溶液,混合液的pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的变化过程中,有共价键明显被破坏的是( )
①I2升华
②NaCl颗粒被粉碎
③HCl溶于水得盐酸
④从NH4HCO3中闻到了刺激性气味.
A.①②
B.②③
C.①④
D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分) 砷(As)是第四周期ⅤA族元素,可以形成As2O3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图。
(2)工业上常将含砷废渣(主要成分为As2O3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式。该反应需要在加压下进行,原因是。
(3)已知:As(s)+ ![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1H2(g)+
H2(g)+2O2(g)=H3AsO4(s) ΔH1H2(g)+ ![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+ ![]() O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =。
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应:AsO33(aq)+I2(aq)+2OH![]() AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。
AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。 
①下列可判断反应达到平衡的是(填标号)。
a.溶液的pH不再变化
b.v(I)=2v(AsO33)
c. c (AsO43)/c (AsO33)不再变化
d. c(I)=y mol·L1
②tm时,v正 v逆(填“大于”“小于”或“等于”)。
③tm时v逆 tn时v逆(填“大于”“小于”或“等于”),理由是。
④若平衡时溶液的pH=14,则该反应的平衡常数K为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com