
【题目】下列各表述与示意图一致的是

A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.根据图②可判断可逆反应A2(g)+3B2(g) ![]() 2AB3(g)的△H<0
2AB3(g)的△H<0
C.图③可表示向Ba(OH)2溶液中加入Na2SO4溶液至过量时溶液导电性的变化
D.图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g) △H>0未使用和使用催化剂时,反应过程中的能量变化
科目:高中化学 来源: 题型:
【题目】
试剂 | 现象 | 结论 | |
A | 金属钠 | 有气体产生 | 含羟基或羧基或羟基、羧基 |
B | 银氨溶液 | 产生银镜 | 含有醛基 |
C | 碳酸氢钠溶液 | 产生气泡 | 含有羧基 |
D | 溴水 | 溶液褪色 | 含有碳碳双键 |
A.A B.B C.C D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
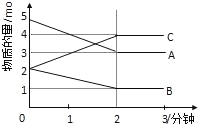
【题目】某可逆反应在某体积为5L的密闭容器中进行,在从0﹣3分钟各物质的量的变化情况如图所示(A、B、C均为气体).
(1)该反应的化学方程式为 ;
(2)反应开始至2分钟时,B的平均反应速率为 .
(3)能说明该反应已达到平衡状态的是 .
a.v(A)=2v(B)
b.容器内压强保持不变
c.v逆(A)=v正(C)
d.容器内混合气体的密度保持不变
(4)由如图求得A的平衡时的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室中制备气体或验证气体性质的装置图

(1)发生装置A中制取氯气的化学方程式 .
(2)利用上图装置制备纯净的氯气,并证明氧化性:C12>Fe3+
则装置B中的溶液的作用是 ;装置D中加的最佳试剂是(填序号) :供选试剂:a.浓H2SO4b.FeCl2溶液 c.无水氯化钙 d.KSCN与FeCl2的混合溶液
(3)在图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置同时完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
证明SO2具氧化性和漂白性:B中为少量Na2S溶液、C中加品红溶液,D中应加入足量的 (填溶液名称),E中加入 溶液(填化学式).
(4)证明碳元素的非金属性比硅元素的强的现象为 ;实验2不严谨之处应如何改进 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的废气中含有CO、SO2、NO等有毒气体,为了更有效地治理该废气,某研究小组分别设计了如下两个方案:
方案(1):治理含CO、SO2的烟道气,以Fe2O3作催化剂,将CO、SO2在380℃时转化为S和一种无毒气体。
已知:ⅰ.硫的熔点112.8℃,沸点444.6℃;
ⅱ.反应每得到1mol硫,放出270kJ的热量。
①写出该治理烟道气反应的热化学方程式: 。
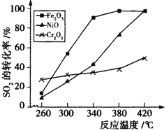
②其他条件相同,催化剂不同时,上述反应中SO2的转化率随反应温度的变化如下图。不考虑催化剂价格因素,生产中选Fe2O3作催化剂的主要原因是 。
方案(2):用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g) ![]() N2(g)+CO2(g)。向某容积为2L 的密闭容器中加入NO和足量的活性炭(固体试样体积忽略不计),恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g)。向某容积为2L 的密闭容器中加入NO和足量的活性炭(固体试样体积忽略不计),恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.32 | 0.32 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.34 | 0.34 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.17 | 0.17 |
①10min~20min以v(CO2)表示的反应速率为 。
②根据表中数据,T1℃时该反应的平衡常数为 (保留两位有效数字)。
③下列各项能作为判断该反应达到平衡状态标志的是 (填序号字母)。
A.容器内压强保持不变
B.2v正(NO)=v逆(N2)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
④30min时改变某一条件,反应重新达到平衡,则改变的条件可能是 ;
⑤一定温度下,随着NO的起始浓度增大,NO的平衡转化率 (填“增大”、“减小”或“不变”)
⑥50min时,保持其他条件不变,往容器中再充入0.32 mol NO和0.34mol CO2,平衡将向 方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型乙醇电池用磺酸类质子作溶剂,电池总反应为:C2H5OH +3O2→2CO2 +3H2O,电池示意图如下图。下面对这种电池的说法正确的是
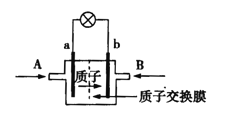
A.A处通氧气,B处通乙醇
B.电池工作时电子由a极沿导线经灯泡再到b极
C.电池正极的电极反应为:O2+2H2O+4e-=4OH-
D.若用这种电池作电源保护金属铁,则a电极连接石墨,b电极连接铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是制取干燥、纯净的氯气并验证氯气的性质的装置(加热及夹持装置省略)。

(1)写出装置A中制备氯气的化学反应方程式: 。
(2)装置C的作用是 。
(3)在反应过程中,装置D内干燥的蓝色石蕊试纸不变色,湿润的蓝色石蕊试纸先变红后退色,使试纸变红的物质是 (填化学式),使试纸退色的物质是 (填化学式)。
(4)装置D内湿润的KI淀粉试纸变蓝,说明Cl的非金属性 I的非金属性(填“大于”或“小于”)。
(5)该实验装置有个明显的缺陷是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银铜合金广泛用于航空工业。从切割废料中回收并制备铜化工产品的工艺如下:

(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为 ;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学方程式为 。
(2)固体混合物B的组成为 ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为 。
(3)完成煅烧过程中一个反应的化学方程式: CuO+ Al2O3![]() CuAlO2+ ↑。
CuAlO2+ ↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为 molCuAlO2,至少需要1.0mol·L-1的Al2(SO4)3溶液 L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是 、过滤、洗涤和干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com