
| A. | 乙苯 | B. | 邻二甲苯 | C. | 间二甲苯 | D. | 对二甲苯 |
科目:高中化学 来源: 题型:多选题
| A. | 已知2C(s)+2O2(g)═2CO2(g);△H1,2C(s)+O2(g)=2CO(g);△H2.则△H1<△H2 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: N2(g)+3H2(g)?$?_{500℃,30MPa}^{催化剂}$2MH3(g),△H=-38.6kJ•mol-1 | |
| C. | 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol | |
| D. | 已知2H2(g)+O2(g)═2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 弱碱性溶液中可能大量存在Na+、K+、Cl?、HCO3? | |
| B. | 在氢氧化铁胶体中能大量存在:H+、K+、S2-、Br- | |
| C. | 由水电离出的c(OH-)=1×10-13mol•L-1的溶液中一定能大量共存:Na+、[Al(OH)4]-、S2-、CO32- | |
| D. | 中性溶液中可能大量存在Fe3+、K+、Cl?、SO42? |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置甲:用于制取并收集乙酸乙酯 | |
| B. | 装置乙:用于分离两种沸点不同的两种物质 | |
| C. | 装置丙:收集二氧化碳,从a口进气b口排气 | |
| D. | 装置丁:可用来制取氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{36.5a}{22.4(a+1)d}$ | B. | $\frac{1000ad}{36.5a+22.4}$ | ||
| C. | $\frac{ad}{36.5a+22400}$ | D. | $\frac{1000ad}{36.5a+22400}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{{W}_{1}+{W}_{2}}{2}$ | B. | <$\frac{{W}_{1}+{W}_{2}}{2}$ | C. | >$\frac{{W}_{1}+{W}_{2}}{2}$ | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中次磷酸根离子得电子,表现还原性 | |
| B. | 该反应中氧化剂与还原剂的物质的量之比为1:1 | |
| C. | 若将硫酸铜溶液换成硝酸银溶液,容器内壁不会形成镀层 | |
| D. | 该反应每消耗3 mol X-,转移电子的物质的量为2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
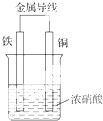
| A. | 铁片上发生氧化反应Fe-3e-═Fe3+ | B. | 铜片上发生还原反应2H++2e-═H2↑ | ||
| C. | 铜片上发生氧化反应Cu-2e-═Cu2+ | D. | 溶液中NO${\;}_{3}^{-}$的浓度基本不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com