
| A. | H2O和H2O2中的化学键类型完全相同 | |
| B. | N2的结构式为N-N | |
| C. | 一个D216O分子所含的中子数为10 | |
| D. | NaCl的电子式为 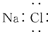 |
分析 A.双氧水分子中含有O-O非极性键;
B.氮气分子中存在氮氮三键;
C.D原子含有1个中子;
D.氯化钠为离子化合物,应该符合离子化合物电子式特点
解答 解:A.水分子中O原子和H原子只存在极性键,双氧水分子中O原子和H原子之间存在极性键、O原子和O原子之间存在非极性键,故A错误;
B.氮气分子中存在氮氮三键,氮气分子的结构式为N≡N,故B错误;
C.D原子中含1个中子、O原子中含有8个中子,所以一个D2O分子所含的中子数为1×2+8=10,故C正确;
D.氯化钠为离子化合物,其电子式为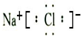 ,故D错误;
,故D错误;
故选C.
点评 本题主要考查了化学用语,属于基础题,涉及结构式、化学键、电子式等知识点,根据这些知识点的书写规则书写,注意离子化合物和共价化合物电子式书写区别,为易错点.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
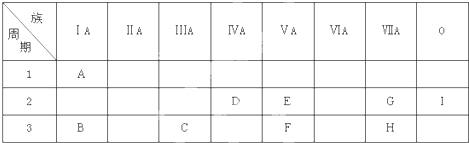
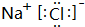 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl | B. | Na2S | C. | Na2O | D. | K2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大烧杯上没有盖硬纸板 | |
| B. | 用环形铜丝搅拌棒代替环形玻璃搅拌棒 | |
| C. | 用相同浓度和体积的硝酸代替稀盐酸溶液进行实验 | |
| D. | 用1gNaOH固体代替50mL0.5mol/L的NaOH溶液进行实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有大量AlO2-的溶液中:K+、Al3+、Br-、HCO3-可共存 | |
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2 CO(g)+O2(g)反应的△H=+566.0kJ/mol | |
| C. | 将SO2通入Ca(ClO)2溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2 HClO | |
| D. | 在某钠盐溶液中含有等物质的量的Cl-、I-、SO32-、CO32-、NO3-、SiO32-中的一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8n | B. | 14n | C. | 18n | D. | 44n |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ⅰ.(1)人们把拆开1mol化学键所吸收的能量看成该化学键的键能.
Ⅰ.(1)人们把拆开1mol化学键所吸收的能量看成该化学键的键能.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com