
反应3Fe(s)+4H2O(g)  Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是
| A.容器内压强不再改变 | B.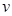 (H2O)= (H2O)=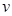 (H2) (H2) |
| C.气体的密度不再改变 | D.反应不再进行 |
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案科目:高中化学 来源: 题型:单选题
在一个体积不变的密闭容器中发生可逆反应:A2(g)+B2(g) 2AB(g),达到平衡的标志是
2AB(g),达到平衡的标志是
A.容器的总压强不随时间而变化 B.容器内气体的密度不再改变
C.单位时间内有nmolA2生成的同时有nmolB2消耗 D. v正(A2)= 2v逆(AB)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在t℃时,10mL0.4mol·L-1H2O2溶液发生催化分解:2H2O2 = 2H2O + O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表
| t /min | 0 | 2 | 4 | 6 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
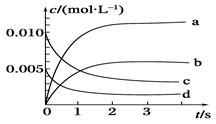
(10分)800℃时在2L密闭容器内反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定温度下,体积固定的密闭容器中进行可逆反应A(g) + 3B(g) 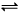 2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是
2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是
A.单位时间内生成n mol A,同时生成3n mol B
B.A、B、C的浓度不再发生变化
C.混合气体的压强不再发生改变
D.C生成的速率与C分解的速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol 在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol 在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4) | 0.50 | 0.30 | 0.18 | …… | 0.15 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关化学反应速率的说法中,正确的是
A.往容积一定的容器中再通入O2,可以加快反应2SO2+O2 2SO3的反应速率 2SO3的反应速率 |
| B.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 |
C.对于C(s)+H2O(g)  CO(g)+H2(g)的反应,加入固体炭,反应速率加快 CO(g)+H2(g)的反应,加入固体炭,反应速率加快 |
| D.100 mL 2 mol·L-1的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
可逆反应:2NO2(g) 2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是
2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO ③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥混合气体的压强不再改变的状态 ⑦混合气体的平均相对分子质量不再改变的状态
| A.①④⑥⑦ | B.②③⑤⑦ |
| C.①③④⑤ | D.全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列事实不能用勒夏特列原理解释的是 ( )
| A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
| B.合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率; |
| C.过氧化氢分解加二氧化锰作催化剂,使单位时间内产生的氧气的量多。 |
| D.久制的氯水PH值变小。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com