
����Ŀ��A��B��C��D��E��FΪ��ѧ��ѧ�еij������ʣ�������A��1��2�ֶ�����Ԫ����ɣ���һ��������������ת����ϵ���������������
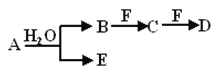
��1����������AΪ��ɫ����
����F��һ�ֽ������ʣ���д��B������F��Ӧ����C������E�����ӷ���ʽ��__________��
����CΪֱ���ͷ��ӣ�E����Ư���ԣ�����F��ɫ��Ӧ�ʻ�ɫ����д����ҵ���Ʊ�����F�Ļ�ѧ��Ӧ����ʽ��__________��
(2)��AΪ����ɫ���壬��A���ʵĵ���ʽΪ��__________��������A��D����Է���������ȣ��������ӷ���ʽ��ʾ����F��ˮ��Һ�����Ե�ԭ��__________��
���𰸡�Fe+4H++NO2=Fe3+NO��+2H2ONH3+CO2+H2O+NaCl=NaHCO3+NH4Cl��2NaHCO3![]() Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2��![]() Al3++3H2O
Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
��������A��B��C��D��E��FΪ��ѧ��ѧ�еij������ʣ�������A��1��2�ֶ�����Ԫ����ɣ���ת����ϵ��֪��B��EΪ������Ԫ����ɣ�
��1������F��һ�ֽ������ʣ���ת����ϵ��֪��FΪ��۽�����ӦΪFe��B��Fe��Ӧ���ɸ�Fe������AΪ��ɫ���壬��ˮ��Ӧ����B��E����AΪ����������BΪ���ᡢEΪNO��CΪ����ͭ��DΪ������������B������F��Ӧ����C������E�����ӷ���ʽΪ��Fe+4H++NO3-=Fe3++NO��+2H2O��
��AΪ��ɫ���壬��ˮ��Ӧ����B��E��E����Ư���ԣ���AΪ������BΪHCl��EΪHClO������F��ɫ��Ӧ�ʻ�ɫ������NaԪ�أ�CΪֱ���ͷ��ӣ����ת����ϵ��֪��FΪ̼���ơ�CΪ������̼��DΪ̼�����ƣ���ҵ���Ʊ�̼���ƵĻ�ѧ��Ӧ����ʽ��NH3+CO2+H2O+NaCl=NaHCO3��+NH4Cl��2NaHCO3![]() Na2CO3+CO2��+H2O��
Na2CO3+CO2��+H2O��
��2��AΪ����ɫ���壬����ˮ��Ӧ����AΪ�������ƣ������ʽΪ��![]() ��������A��D����Է���������ȣ����ת����ϵ��BΪ�������ơ�CΪƫ�����ơ�FΪ���Ρ�DΪ����������EΪ�����������ӷ���ʽ��ʾ����F��ˮ��Һ�����Ե�ԭ��Ϊ��Al3++3H2O
��������A��D����Է���������ȣ����ת����ϵ��BΪ�������ơ�CΪƫ�����ơ�FΪ���Ρ�DΪ����������EΪ�����������ӷ���ʽ��ʾ����F��ˮ��Һ�����Ե�ԭ��Ϊ��Al3++3H2O![]() Al��OH��3+3H+��
Al��OH��3+3H+��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��a��ʵ���ҳ����ü�ȩ���ⶨ(NH4)2SO4��Ʒ�е��������������䷴Ӧԭ��Ϊ��4NH4����6HCHO��3H����6H2O��(CH2)6N4H�����ζ�ʱ��1mol (CH2)6N4H����1mol H���൱����Ȼ����NaOH����Һ�ζ���Ӧ���ɵ��ᡣij��ȤС���ü�ȩ������������ʵ�飺
����I����ȡ��Ʒ1.500g��
�������Ʒ�ܽ����ȫת�Ƶ�250mL����ƿ�У����ݣ����ҡ�ȡ�
�������ȡ25.00mL��Ʒ��Һ��250mL��ƿ�У�����10mL20�������Լ�ȩ��Һ��ҡ�ȡ�����5min����1��2�η�̪��Һ����NaOH����Һ�ζ����յ㡣�����������������ظ�2�Ρ�
��1�����ݲ������գ�
��ѡ�õζ���Ϊ ����ס����ҡ�����


�ڼ�ʽ�ζ���������ˮϴ�Ӻ�ֱ�Ӽ���NaOH����Һ���еζ���������Ʒ�е����������� ���ƫ�ߡ�����ƫ�͡�����Ӱ�족������ƿ������ˮϴ�Ӻ�ˮδ��������ζ�ʱ��ȥNaOH����Һ����� ���ƫ����ƫС������Ӱ�족����
�۵ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲� ��
A���ζ�����Һ��ı仯 B����ƿ����Һ��ɫ�ı仯
�ܵζ��ﵽ�յ�ʱ����ָ̪ʾ���� ɫ��� ɫ��
��2���ζ�������±���ʾ��
�ζ����� | ������Һ�����/mL | ����Һ����� | |
�ζ�ǰ�̶�/mL | �ζ���̶�/mL | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
��NaOH����Һ��Ũ��Ϊ0.1010mo1�� L��1�������Ʒ�е�����������Ϊ ��
b ���ڲⶨ�к��ȵ�ʵ���У�����˵����ȷ���ǣ� ��
A��ʹ�û��β�������Ϊ�˼ӿ췴Ӧ���ʣ���Сʵ�����
B��Ϊ��ȷ�ⶨ��Ӧ�����Һ���¶ȣ�ʵ�����¶ȼ�ˮ����Ӧ��С�ձ��ײ��Ӵ�
C����0.5mol��L-1NaOH��Һ�ֱ���0.5 mol��L-1�����ᡢ������Һ��Ӧ������ȡ����Һ�����ȣ����õ��к�����ֵ��ͬ
D���ڲⶨ�к���ʵ������Ҫʹ�õ������У���ƽ����Ͳ���ձ����ζ��ܡ��¶ȼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.ij�¶�ʱ����һ��10L�ĺ��������У�X��Y��Z��Ϊ���壬�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ��������գ�

��1���÷�Ӧ�Ļ�ѧ����ʽΪ____________________��
��2����Ӧ��ʼ��2min��������Z��ʾ��ƽ����Ӧ����Ϊ______________________��
��3��ƽ��ʱ�����ڻ�������ܶȱ���ʼʱ__________������������������С�������������ͬ������������ƽ����Է�����������ʼʱ___________��
��4����a mol X��b mol Y�Ļ�����巢��������Ӧ����Ӧ��ijʱ�̸����ʵ���ǡ�����㣺
n��X��=n��Y��=2n��Z������ԭ���������a��b=___________��
�����ں��º��ݵ��ܱ������У����������������ٷ����仯ʱ������������ѹǿ�������������ܶȣ����������������ʵ���������������ƽ����Է���������������������ɫ��������Ӧ���������ķ�Ӧ����֮�ȵ��ڻ�ѧ������֮��
��1��һ����֤��2SO2(g)��O2(g)![]() 2SO3(g)�ﵽƽ��״̬����_______������ţ���ͬ����
2SO3(g)�ﵽƽ��״̬����_______������ţ���ͬ����
��2��һ����֤��I2(g)��H2(g)![]() 2HI(g)�ﵽƽ��״̬���� _________��
2HI(g)�ﵽƽ��״̬���� _________��
��3��һ����֤��A(s)��2B(g)![]() C(g)��D(g)�ﵽƽ��״̬����________��
C(g)��D(g)�ﵽƽ��״̬����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���ǣ�
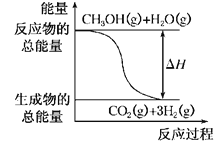
��CH3OH��g����H2O��g��=CO2��g����3H2��g�� ��H����49.0 kJ��mol��1
��CH3OH��g����![]() O2��g��=CO2��g����2H2��g�� ��H����192.9 kJ��mol��1
O2��g��=CO2��g����2H2��g�� ��H����192.9 kJ��mol��1
����˵����ȷ������ ��
A��CH3OH��ȼ����Ϊ��192.9 kJ��mol��1
B����Ӧ���е������仯����ͼ��ʾ
C��CH3OHת���H2�Ĺ���һ��Ҫ��������
D��������֪��ӦCH3OH��l����![]() O2��g��=CO2��g����2H2��g����H >��192.9 kJ��mol��1
O2��g��=CO2��g����2H2��g����H >��192.9 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���������²��ϣ�ͭƬ����Ƭ��ʯī����CuCl2��Һ��FeCl3��Һ�����ߡ�������������(װ����֬-KCl��U�ι�)���ձ�������ͬѧ�������ͼ1��ԭ���װ��������ͬѧ���ּ�ͬѧ��Ƶ�ԭ���װ��Ч�ʲ��ߣ������ڶ�ʱ���ھͻ�˥����Ϊ����������⣬��ԭ�����Ƴ��������ŵ�װ�ã���ͼ2��ʾ��
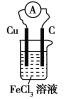
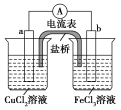
ͼ1 ͼ2
��1������ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���___________������ţ���ͬ����
a��C(s)+H2O(g)=CO(g)+H2(g) ��H>0
b��2H2(g)+O2(g)=2H2O(l) ��H<0
c��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ��H<0
����ͬѧ��Ƶ�ԭ��أ�����ʯī����Ϊ��Ƭ�����ܵ缫��Ӧʽ�Ƿ��ı䣬������д���ı���ܵĵ缫��Ӧʽ����������д��������_______________________��
����ͬѧ��Ƶ�ԭ����缫��Ӧ�����ͬ������ص�Ч�ʸߺܶࡣ��ͬѧ��Ƶ�ԭ������缫�ֱ�Ϊ��a��_______������ͭƬ������Ƭ������ʯī��������ͬ����b��__________�������ĵ缫��ӦʽΪ___________________�������ĵ缫��ӦʽΪ____________________��
��2��������ͬѧ��Ƶ�ԭ��أ�����˵������������____________��
a��ʵ������У�����ձ���ClŨ������
b��ʵ�������ȡ�����ţ�ԭ������ܼ�������
c������ͨ�����Ŵ��Ҳ��ձ���������ձ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��� pH=3 �������� pH=9 �� NaOH ��Һ��ϣ���Ҫ�õ� pH = 7 ����Һ�����ʱ������ NaOH ��Һ�������Ϊ�� ��
A.1: 200 B. 200 : 1 C. 100 : 1 D.1��100
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������������H+��[c��OH�����ɺ���]����Na+��Cl����NH4+��SO42����Ũ������Ϊ��c��Na+��=2.3��10��5mol/L��c��Cl����=3.5��10��5mol/L��c��NH4+��=2.3��10��5mol/L��c��SO42����=1.05��10��5mol/L����õ������pHΪ��������
A. 3 B. 4 C. 5 D. 6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϲ��ؾ��п��������ס��������������������ã����Ľṹ��ʽ����ͼ��ʾ�������й������ϲ��ص�˵���������
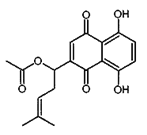
A. �÷����к���1������̼ԭ��
B. ����FeCl3��Һ������ɫ��Ӧ
C. 1mol �����ϲ���������2molBr2��Ӧ
D. 1mol�����ϲ���������2molNaOH��Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com