
 ��֪A��B��C��D��E����Ԫ�����ڱ���ǰ36�ŵ�Ԫ�أ����ǵ�ԭ��������������Aԭ�ӻ�̬ʱ���������������ڲ����������2����Bԭ�ӻ�̬ʱs��������P��������ȣ�C��Ԫ�����ڱ��ĸ�Ԫ���е縺�����D�Ļ�̬ԭ�Ӻ�����6���ܼ���ȫ���������ӣ�Eԭ�ӻ�̬ʱδ�ɶԵ�������ͬ����Ԫ�������ģ�
��֪A��B��C��D��E����Ԫ�����ڱ���ǰ36�ŵ�Ԫ�أ����ǵ�ԭ��������������Aԭ�ӻ�̬ʱ���������������ڲ����������2����Bԭ�ӻ�̬ʱs��������P��������ȣ�C��Ԫ�����ڱ��ĸ�Ԫ���е縺�����D�Ļ�̬ԭ�Ӻ�����6���ܼ���ȫ���������ӣ�Eԭ�ӻ�̬ʱδ�ɶԵ�������ͬ����Ԫ�������ģ�| 4+2-2��3 |
| 2 |
| 4+2-2��3 |
| 2 |
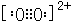 ��1mol O22+�к��еĦм���ĿΪ2NA���ʴ�Ϊ��
��1mol O22+�к��еĦм���ĿΪ2NA���ʴ�Ϊ��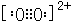 ��2��
��2��| 1 |
| 8 |
| 1 |
| 2 |
| 78 |
| NA |
| ||
| ag/cm3 |
| 78��4 |
| aNA |
| 78��4 |
| aNA |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��H+�����¶ȵ����߶����� |
| B��ˮ�ĵ�������Ƿ��ȵ� |
| C��ˮ�ĵ���ƽ�ⳣ����Ũ�ȡ��¶��й� |
| D����35��ʱ��c��H+����c��OH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ڢۢ� | C���ۢ� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
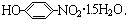 ��
�� ���ĵ���ƽ�ⳣ��K2����Դ�С
���ĵ���ƽ�ⳣ��K2����Դ�С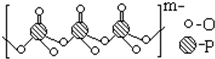
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
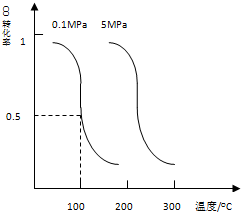
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
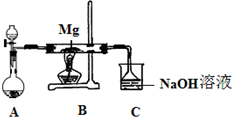 SiO2��SO2��CO2����������������ǵĻ�ѧ���ʾ���һ���������ԣ�Mg��Na�Ļ�ѧ����Ҳ����һ�������ԣ�ij��ȤС������ͼ��ʾװ�ý���Mg��SO2��Ӧ��ʵ�飮
SiO2��SO2��CO2����������������ǵĻ�ѧ���ʾ���һ���������ԣ�Mg��Na�Ļ�ѧ����Ҳ����һ�������ԣ�ij��ȤС������ͼ��ʾװ�ý���Mg��SO2��Ӧ��ʵ�飮
| ||
| ||
| ��� | ʵ�鲽�� | Ԥ������ͽ��� |
| �� | ȡ������Ӧ�����ù������Թ��� | |
| �� | ���Թ��еĹ��������μ� �Թܿ����ϴ����ܵĵ���������������ͨ��ʢ�� |
���Թ��е� ���ͬѧ�Ʋ���ȷ�� ���Թ��еĹ���δ��ȫ�ܽ⣬�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ΪNA��NO2��CO2��������к��е���ԭ����Ϊ2NA |
| B��1mol/L��NaCl��Һ�У�Na+�����ʵ�����1mol H2 |
| C��18g H2O�ڱ�״���µ������22.4L |
| D���ڱ�״��ʱ��20mL NH3��60mL O2�����ķ��Ӹ�����Ϊ2��1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com