
 E、G、M、Q、T是五种原子序数依次增大的前四周期元素.E、G、M是位于P区的同一周期的元素,M的价层电子排布为nsnnp2n,E与M原子核外的未成对电子数相等;QM2与GM2-为等电子体;T为过渡元素,其原子核外没有未成对电子.请回答下列问题:
E、G、M、Q、T是五种原子序数依次增大的前四周期元素.E、G、M是位于P区的同一周期的元素,M的价层电子排布为nsnnp2n,E与M原子核外的未成对电子数相等;QM2与GM2-为等电子体;T为过渡元素,其原子核外没有未成对电子.请回答下列问题: .E、M电负性相差1.0,由此可以判断EM应该为极性较强的分子,但实际上EM分子的极性极弱,请解释其原因从电负性分析,CO中的共用电子对偏向氧原子,但分子中形成配位键的电子对是由氧原子单方面提供的,抵消了共用电子对偏向O而产生的极性.
.E、M电负性相差1.0,由此可以判断EM应该为极性较强的分子,但实际上EM分子的极性极弱,请解释其原因从电负性分析,CO中的共用电子对偏向氧原子,但分子中形成配位键的电子对是由氧原子单方面提供的,抵消了共用电子对偏向O而产生的极性.分析 E、G、M、Q、T是五种原子序数依次增大的前四周期元素,E、G、M是位于P区的同一周期的元素,M的价层电子排布为nsnnp2n,s能级最多排列2个电子,则n=2,所以M价层电子排布式为2s22p4,为O元素;E与M原子核外的未成对电子数相等,则E是C元素,G为N元素;QO2与NO2-为等电子体,则Q为S元素;T为过渡元素,其原子核外没有未成对电子,则T为Zn元素;
(1)与T同区、同周期元素为Cu元素,其原子核外有29个电子,3d、4s能级电子为其价电子,根据构造原理书写该原子价电子排布式;
(2)C、N、O均可与氢元素形成氢化物,它们的最简单氢化物在固态时都形成分子晶体,干冰和甲烷晶胞都是面心立方晶胞结构;
(3)C、N、O的最简单氢化物中,其氢化物空间构型分别是正四面体、三角锥形、V形,其键角依次减小;其中N的最简单氢化物的VSEPR模型名称为正四面体,O的最简单氢化物的分子立体构型名称为V形;
(4)CO、NO+、N2互为等电子体,等电子体结构相似;
C、O电负性相差1.0,由此可以判断CO应该为极性较强的分子,但实际上CO分子的极性极弱,根据电子对的偏向分析解答;
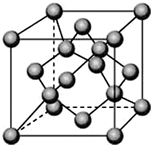
(5)ZnS晶体结构如图所示,该晶胞中黑色球个数是4、白色球个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶胞质量为$\frac{4M}{{N}_{A}}$g,根据V=$\frac{m}{ρ}$计算晶胞体积,再计算晶胞棱长,ab之间距离为该晶胞体对角线长的$\frac{1}{4}$.
解答 解:E、G、M、Q、T是五种原子序数依次增大的前四周期元素,E、G、M是位于P区的同一周期的元素,M的价层电子排布为nsnnp2n,s能级最多排列2个电子,则n=2,所以M价层电子排布式为2s22p4,为O元素;E与M原子核外的未成对电子数相等,则E是C元素,G为N元素;QO2与NO2-为等电子体,则Q为S元素;T为过渡元素,其原子核外没有未成对电子,则T为Zn元素;
(1)与T同区、同周期元素为Cu元素,其原子核外有29个电子,3d、4s能级电子为其价电子,根据构造原理书写该原子价电子排布式为3d104s1,故答案为:3d104s1;
(2)C、N、O均可与氢元素形成氢化物,它们的最简单氢化物在固态时都形成分子晶体,干冰和甲烷晶胞都是面心立方晶胞结构,氨气、水分子之间存在氢键,则与干冰晶胞结构不同的是NH3、H2O,故答案为:NH3、H2O;
(3)C、N、O的最简单氢化物中,其氢化物空间构型分别是正四面体、三角锥形、V形,其键角依次减小,即键角大小顺序是CH4>NH3>H2O;其中N的最简单氢化物中N原子价层电子对个数是4,则氨气分子的VSEPR模型名称为正四面体,O的最简单氢化物是水,水分子中O原子价层电子对个数是4且含有一个孤电子对,所以水分子立体构型名称为V形,
故答案为:CH4>NH3>H2O;正四面体;V形;
(4)CO、NO+、N2互为等电子体,等电子体结构相似,则CO分子结构式为 ;
;
C、O电负性相差1.0,由此可以判断CO应该为极性较强的分子,但实际上CO分子的极性极弱,从电负性分析,CO中的共用电子对偏向氧原子,但分子中形成配位键的电子对是由氧原子单方面提供的,抵消了共用电子对偏向O而产生的极性,
故答案为: ;从电负性分析,CO中的共用电子对偏向氧原子,但分子中形成配位键的电子对是由氧原子单方面提供的,抵消了共用电子对偏向O而产生的极性;
;从电负性分析,CO中的共用电子对偏向氧原子,但分子中形成配位键的电子对是由氧原子单方面提供的,抵消了共用电子对偏向O而产生的极性;
(5)ZnS晶体结构如图所示,该晶胞中黑色球个数是4、白色球个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶胞质量为$\frac{4M}{{N}_{A}}$g,则晶胞V=$\frac{4M}{{N}_{A}}$g÷ρg/cm3=$\frac{4M}{ρ{N}_{A}}$cm3,则晶胞棱长=$\root{3}{\frac{4M}{ρ{N}_{A}}}$cm,
ab之间距离为该晶胞体对角线长的$\frac{1}{4}$=$\frac{1}{4}$×$\sqrt{3}$×=$\root{3}{\frac{4M}{ρ{N}_{A}}}$cm=$\frac{\sqrt{3}}{4}×\root{3}{\frac{4M}{ρ{N}_{A}}}$cm,
故答案为:$\frac{\sqrt{3}}{4}×\root{3}{\frac{4M}{ρ{N}_{A}}}$.
点评 本题考查物质结构和性质,涉及晶胞计算、原子杂化方式判断、分子空间构型判断、原子核外电子排布等知识点,难点是晶胞计算中ab距离与晶胞体对角线长关系,需要学生具备一定的空间想象与数学计算能力,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 已知A、B、C、D都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他3种元素既不在同一周期又不在同一主族.B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D原子的L层电子数与最外层电子数之比为4:1,其d轨道中有一对成对电子.请回答:
已知A、B、C、D都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他3种元素既不在同一周期又不在同一主族.B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D原子的L层电子数与最外层电子数之比为4:1,其d轨道中有一对成对电子.请回答: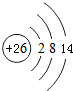 ,它的+3价离子的电子排布式为1s22s22p63s2sp5.
,它的+3价离子的电子排布式为1s22s22p63s2sp5.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | |
| B. | 石油裂解、煤的气化、海水制镁等过程中都包含化学变化 | |
| C. | 煤经气化、液化和干馏三个物理变化过程,可变为清洁能源 | |
| D. | 通过化学变化可以实现235U与238U的相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
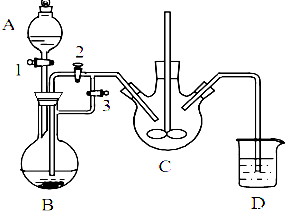 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
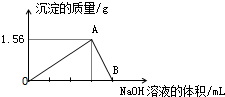 向40mL某AlCl3溶液中滴加2mol•L-1的NaOH溶液时,得到Al(OH)3沉淀的质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
向40mL某AlCl3溶液中滴加2mol•L-1的NaOH溶液时,得到Al(OH)3沉淀的质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A. | 在冰醋酸中,高氯酸的酸性最强 | |
| B. | 水对于这四种酸的强弱没有区分能力,但醋酸可以区分这四种酸的强弱 | |
| C. | 在冰醋酸中1mol/L的高氯酸的电离度约为0.4% | |
| D. | 在冰醋酸中硫酸的电离方程式为:H2SO4═2H++SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com