
【题目】用如图所示装置进行下列实验,其中不合理的是

A.用CCl4萃取碘水中的碘B.用NaOH溶液除去溴苯中的溴
C.用水除去硬脂酸钠中的甘油D.用饱和Na2CO3溶液除去乙酸乙酯中的乙酸
【答案】C
【解析】
由图可知,为萃取、分液装置,可分离溶质在不同溶剂中溶解性差异大的混合物,或分离分层的液体,以此来解答。
A、用CCl4萃取碘水中的碘的实验操作为萃取、分液,可通过该装置完成,故A不符合题意;
B、溴苯在水中溶解度较小,溴在溴苯中溶解度较大,向溴苯与溴的溶液中加入NaOH溶液后,溴与NaOH反应,生成无机盐,无机盐易溶于水,难溶于溴苯,可分层,然后通过分液分离出溴苯,故B不符合题意;
C、硬脂酸钠、甘油均溶于水,不能利用图中装置分离,故C符合题意;
D、乙酸与碳酸钠反应后,与乙酸乙酯分层,可利用图中装置、饱和Na2CO3溶液除去乙酸乙酯中的乙酸,故D不符合题意;
故答案为C。


科目:高中化学 来源: 题型:
【题目】已知:2RCH2CHO![]() RCH2CH=CRCHO+H2O;水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下:
RCH2CH=CRCHO+H2O;水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下:

请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%。则A的分子式为_________;结构分析显示A只有一个甲基,A的名称为___________。
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为___________________。
(3)C有____种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂:______________________________________________________;
(4)第③的反应类型为_________________;D所含官能团的名称为________________。
(5)写出同时符合下列条件的水杨酸所有同分异构体的结构简式:_________________________。
a.分子中含有6个碳原子在一条线上 b.分子中所含官能团包括水杨酸具有的官能团
(6)第④步的反应条件为___________;写出E的结构简式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际气候变化经济学报告中显示,大气中CO2浓度每增加一倍,可使地表平均温度上升56℃。为减少温室效应的加剧,需将工业生产中产生的CO2分离出来加以利用。回答下列问题:
(1)在500℃时,Li4SiO4与低浓度的CO2反应生成两种锂盐,待该反应达到化学反应的限度后,升温至700℃,两种锂盐反应放出高浓度的CO2,而Li4SiO4可循环利用。写出700℃时两种锂盐反应的化学方程式___。
(2)CO2与NH3反应可合成化肥。
①已知:2NH3(g)+CO2(g)=NH2COONH4(s) △H=-159.5kJmol-1
NH2COONH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5kJmol-1
H2O(l)=H2O(g) △H=+44.0kJmo1-1
则CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的△H=___kJmol-1
②将足量CO2通入饱和氨水中可制得碳铵(NH4HCO3)。已知室温下Kb(NH3H2O)=1.8×10-5,Ka1(H2CO3)=4.3×10-7,则0.0.1molL-1NH4HCO3溶液室温下呈___ (填“酸性”、“中性”或“碱性”)。
(3)在一定条件下,CO2与H2可用于合成甲醇:CO2(g)+3H2(g)CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比[![]() ]达平衡时CO2的转化率[α(CO2)]如图1所示。
]达平衡时CO2的转化率[α(CO2)]如图1所示。
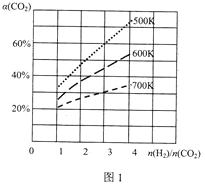
该反应的△H___0(填“>”、“=”或“<”)。
②500K、投料比[![]() ]=3时,H2的平衡转化率为___;设总压强为P0,则化学平衡常数Kp=___(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
]=3时,H2的平衡转化率为___;设总压强为P0,则化学平衡常数Kp=___(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③直接甲醇燃料电池(DMFC)具备低温快速启动、燃料洁净环保以及电池结构简单等特性。该电池使用合适的合金为电极,以氢氧化钠溶液、甲醇、空气为原料。写出其负极电极反应式___。
(4)在TiO2/Cu2Al2O4为催化剂时,CO2和CH4可反应生成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图2所示。300℃400℃时,影响乙酸生成速率的主要因素是___(填“温度”或“催化剂”)。
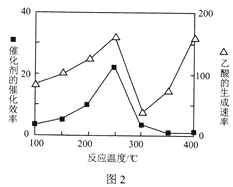
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | n (H2O)/ mol |
0 | 1.20 | 0.60 |
t1 | 0.20 | |
t2 | 0.80 |
依据题意回答下列问题:
(1)反应在t1min内的平均速率为v(H2)=____________mol·L-1·min-1
(2)保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时,n(CO2)=____________mol。
(3)温度升至800℃,上述反应平衡常数为0.64,则正反应为__________反应(填“放热”或“吸热”)。
(4)700℃时,向容积2L的密闭容器中充入CO(g)、H2O(g)、CO2(g)、H2(g)的物质的量分别为1.20mol、2.00mol、1.20mol、1.20mol,则此时该反应v(正)______v(逆)(填“>”、“<”或“=”)。
(5)若该容器体积不变,能判断反应达到平衡的是_______________。
①c(CO)与c(H2)的比值保持不变;②v(CO2)正=v(H2O)逆;③体系的压强不再发生变化;④混合气体的密度不变;⑤体系的温度不再发生变化;⑥气体的平均相对分子质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是网络表情包“苯宝宝装纯(醇)”,该分子由“苯宝宝”与羟基相连,下列说法正确的是
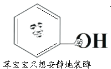
A.该分子属于醇B.该分子中含有两种含氧官能团
C.该物质在空气中放置一段时间会变为粉红色D.该分子苯环上的一个氢原子被丙基(-C3H7)取代所得的同分异构体最多有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用Al-PMOF可快速将芥子气降解为无毒物质,其结构如图。其中X、Y、Z为短周期元素且原子序数依次增大,X、Y同主族。下列说法正确的是
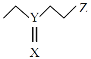
A.简单离子半径:Z>Y>XB.最简单氢化物稳定性:Z>Y>X
C.含氧酸酸性:Z>YD.YXZ2中Y的化合价为+4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某水系锂离子电池可实现Li+和Co2+分离回收,其装置如图。25℃时,Co(OH)2的Ksp分别为6.31×10—15,LiOH的溶解度为12.7g.下列说法不正确的是
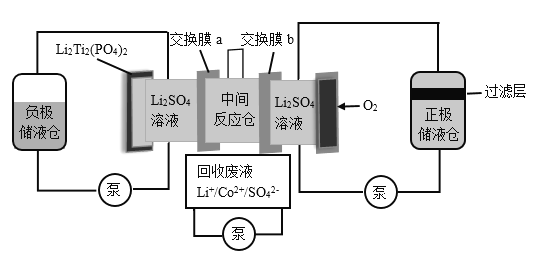
A.负极材料中发生变价的元素是Ti
B.交换膜a为阳离子交换膜
C.负极液和正极液中的c(Li+)均变大
D.在过滤层可收集到Co(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将![]() 通入适量NaOH溶液中,产物中可能含有NaCl、NaClO、
通入适量NaOH溶液中,产物中可能含有NaCl、NaClO、![]() ,且
,且 的值与温度高低有关。当
的值与温度高低有关。当![]() mol时,下列说法不正确的是( )
mol时,下列说法不正确的是( )
A.参加反应的氯气的物质的量等于![]()
B.改变温度,产物中![]() 的最大理论产量为
的最大理论产量为![]()
C.改变温度,反应中转移电子的物质的量![]() 的范围为
的范围为![]()
D.若某温度下,反应后 ,则溶液中
,则溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于0.1 mol·L-1氨水的叙述正确的是
A.加入少量氯化钠溶液,平衡不移动
B.加入少量NaOH固体,平衡正向移动
C.通入少量氯化氢气体,平衡正向移动
D.加入少量MgSO4固体,抑制NH3·H2O电离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com