
实验室用铅蓄电池作电源电解饱和食盐水制取Cl2,已知铅蓄电池放电时发生如下反应:负极:Pb+SO-2e-===PbSO4 正极:PbO2+4H++SO+2e-===PbSO4+2H2O今欲制得Cl2 0.050 mol,这时电池内消耗的H2SO4的物质的量至少是( )
A.0.025 mol B.0.050 mol C.0.100 mol D.0.20 mol
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二下期中化学试卷(解析版) 题型:选择题
草酸二酯(CPPO)结构简式如右图,下列说法正确的是( )
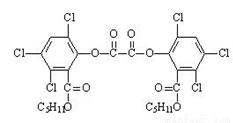
A.草酸二酯的分子式为C26H22Cl6O8
B.1mol草酸二酯与氢氧化钠稀溶液反应时(苯环上卤素不水解),最多消耗6mol NaOH
C.草酸二酯酸性条件下水解可以得到两种有机物
D.1mol草酸二酯与氢气完全反应,需要氢气10mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南衡阳一中高一下期中化学试卷(解析版) 题型:选择题
某元素原子的最外层电子数是次外层的a倍(a>1),则该原子的核内质子数是( )
A.2a+2 B.2a+10 C.a+2 D.2a
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:填空题
(1)为清理路面积雪人们常使用一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。该融雪剂的化学式是____________,该物质中化学键类型是___________,电子式是_________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为______(名称),Y为_______(元素符号),Z原子结构示意图为____________。
②N的最高价氧化物的水化物的化学式为_______________________。
③工业上制取单质M的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:选择题
电解质量分数为5.2%的NaOH溶液1 L(密度为1.06 g/cm3),用铂作电极电解,当溶液中NaOH的质量分数改变了1.0% 时停止电解,此时溶液中符合下表关系的是( )
NaOH的质量分数 | 阳极析出物质的质量/g | 阴极析出物质的质量/g | |
A | 6.2% | 19 | 152 |
B | 6.2% | 152 | 19 |
C | 4.2% | 1.2 | 9.4 |
D | 4.2% | 9.4 | 1.2 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:选择题
SF6是一种优良的绝缘气体,分子结构中只存在S—F键。已知:1 mol S(s)转化为气态硫原子吸收能量280 kJ,断裂1 mol F—F、S—F键需吸收的能量分别为160 kJ、330 kJ。则S(s)+3F2(g)=SF6(g)的反应热ΔH为( )
A.-1780 kJ/mol B.-1220 kJ/mol C.-450 kJ/mol D.+430 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:选择题
已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”。关于标有“+”的接线柱,下列说法中正确的是( )
A.充电时作阳极,放电时作正极 B.充电时作阳极,放电时作负极
C.充电时作阴极,放电时作负极 D.充电时作阴极,放电时作正极
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:选择题
已知:乙醇可被强氧化剂氧化为乙酸,BrCH2CH=CHCH2Br可经三步反应制取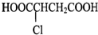 ,其中第二步的反应类型是( )
,其中第二步的反应类型是( )
A.水解反应 B.加成反应 C.氧化反应 D.消去反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北武邑中学高一下5.15周考化学试卷(解析版) 题型:填空题
氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、按盐和纯碱等的原料。
(1)以氨为燃料,氧气为氧化剂可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用。若电极材料均为惰性电极,KOH 溶液作电解质溶液,则该电池负极电极反应式为_______________;正极反应式为______________。
(2)下列措施可以加快合成氨反应速率的是______________。
A.通过缩小容器的容积增大压强 B.及时将氨液化分离出去
C.适当升温 D.添加合适的催化剂
E.恒温恒容时,再充入一定体积的氮气
(3)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入lmolN2 和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
则①从反应开始到25min时,以N2表示的平均反应速率为________;
②H2的平衡转化率为_______________;
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);△H=-159.47kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);△H=+116kJ·mol-1
③ H2O(l)=H2O(g);△H=+44kJ·mol-1
写出CO2 与NH3 合成尿素和液态水的热化学反应方程式_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com