
��4mol A�����2mol B������2L�������л�ϲ���һ�������·������·�Ӧ��2A(g)+B(g) 2C(g)����2s����C��Ũ��Ϊ0.6mol�ML���������м���˵����
2C(g)����2s����C��Ũ��Ϊ0.6mol�ML���������м���˵����
��������A��ʾ�ķ�Ӧƽ������Ϊ0.3mol�M(L��s)��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0. 6 mol�M(L��s)��2sʱ����A��ת����Ϊ70% ��2sʱ����B��Ũ��Ϊ0. 7mol-L-l������ȷ����
| A���ۢ� | B���ڢ� | C���٢� | D���٢� |
C
�������������V(C)=��C�M��t=(0.6mol�ML)�M2s=0.3mol�M(L��s).����ͬһ��ѧ��Ӧ�����ʵ����ʹ�ϵ:V(A) :V(B) :V(C)=2:1:2�ɵ�V(A)=" V(C)=" 0.3mol�M(L��s).����ȷ��V(B) =��1�M2����V(C)= ��1�M2����0.3mol�M(L��s)="0.15" mol�M(L��s) �ڴ���2sʱ����A��ת�����ǣ�{0.3mol�M(L��s) ��2s }�M(4mol��2L) ��100%=30%.����2sʱ����B��Ũ��Ϊ(2mol��2L)- 0.15 mol�M(L��s) ��2s="0.7" mol�ML����ȷ��
���㣺���黯ѧ��Ӧ���ʵĶ��弰��ͬһ����ѧ��Ӧ���ò�ͬ��������ʾ�Ļ�ѧ��Ӧ���ʹ�ϵ��֪ʶ��


 �ŵ������ϵ�д�
�ŵ������ϵ�д� 53������ϵ�д�
53������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�Կ��淴Ӧ2A(s)��3B(g)  C(g)��2D(g) ��H��0����һ�������´ﵽƽ�⣬�����й�������ȷ����
C(g)��2D(g) ��H��0����һ�������´ﵽƽ�⣬�����й�������ȷ����
������A������ƽ��������Ӧ�����ƶ�
�������¶ȣ�ƽ�����淴Ӧ�����ƶ���v(��)��С
��ѹǿ����һ����ƽ�ⲻ�ƶ���v(��)��v(��)����
������B��Ũ�ȣ�v(��)��v(��)
�ݼ��������B��ת�������
| A���٢� | B���� | C���� | D���ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
2012�����������е���192����,���������У�����ƽ���ƶ�ԭ�����͵��� ( )
| A������ɫ��NO2����ѹ����ɫ�ȱ�����dz |
| B����ѹ�ȳ�ѹ�����ںϳ�SO3�ķ�Ӧ |
| C����H2(g)��I2(g)��HI(g)������ɵ�ƽ����ϵ��ѹ����ɫ���� |
| D������ɫ����ˮ���պ���ɫ��dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ڻ�ѧ��Ӧ3W(g)+2X(g)��4Y(g)+3Z(g)�����з�Ӧ���ʹ�ϵ�У���ȷ����
A��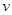 (W)��3 (W)��3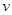 (Z) (Z) | B��2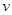 (X)��3 (X)��3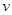 (Z) (Z) |
C��2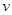 (X)�� (X)��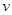 (Y) (Y) | D��3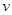 (W)��2 (W)��2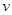 (X) (X) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
COCl2(g) 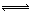 CO(g) + Cl2(g) ��H>0 ����Ӧ�ﵽƽ��ʱ�����д�ʩ�������� �ں���ͨ��������� ������CO��Ũ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2 �ֽ��ʵ���
CO(g) + Cl2(g) ��H>0 ����Ӧ�ﵽƽ��ʱ�����д�ʩ�������� �ں���ͨ��������� ������CO��Ũ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2 �ֽ��ʵ���
| A���٢ܢ� | B���٢ڢ� | C���ڢۢ� | D���ۢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ס��������ݻ���Ϊ1L�ĺ����ܱ������У��ֱ����2mol A��2 mol B��1 mol A��1 mol B����ͬ�����£��������з�Ӧ��A(g)+B(g)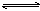 xC(g)
xC(g) 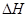 ��0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ��
��0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ��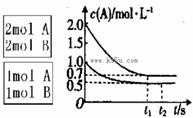
����˵������ȷ����
A��x���ܵ���2Ҳ���ܵ���1
B����ƽ����������г��뺤����ʹc(A)����
C�����������������¿�ʹ�������ڸ����ʵ����������������ڵ���ͬ
D��������������ٳ���2mol A��2 mol B����ƽ��ʱ��������0��7 mol��n(B)��1��4 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��C(s)+CO2(g) 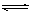 2CO(g)��Ӧ�п�ʹ��Ӧ��������Ĵ�ʩ��
2CO(g)��Ӧ�п�ʹ��Ӧ��������Ĵ�ʩ��
����С�����������������̼��������ͨ��CO2���ܺ�ѹ�³���N2���ݺ����³���N2����ͨ��CO
| A���٢ۢ� | B���ڢܢ� | C���٢ۢ� | D���ۢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ��������������������۷�Ӧʱ��Ϊ�˼�����Ӧ���ʣ��Ҳ�Ӱ���������������������������м���������
| A��NaOH���� | B����������ͭ���� | C��H2O | D������NaCl���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ���¶��£����ݻ�Ϊ2 L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯��ͼ��ʾ���Ը÷�Ӧ���ƶϺ������ǣ� ��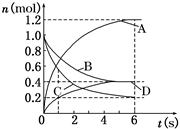
A����Ӧ���е�6 sʱ�������ʵķ�Ӧ�������
B����Ӧ���е�1 sʱ��v (A)��v (C)
C����Ӧ���е�6 sʱ��B��ƽ����Ӧ����Ϊ0.1 mol/(L��s)
D���÷�Ӧ�Ļ�ѧ����ʽΪ3B��4 C 6A��2D
6A��2D
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com