
 CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1 CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1 CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1 CH3OCH3(g) + CO2 (g)的ΔH= ___________;
CH3OCH3(g) + CO2 (g)的ΔH= ___________; CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
 C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为 、
、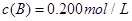 及
及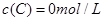 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。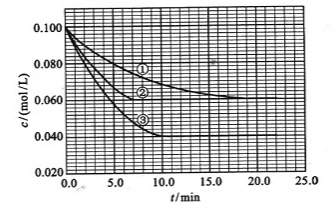
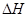 _________0,判断其理由是__________________________________;
_________0,判断其理由是__________________________________; CH3OCH3(g) + CO2 (g),故△H=2△H1+△H2+△H3="-246.4kJ·" mol -1。
CH3OCH3(g) + CO2 (g),故△H=2△H1+△H2+△H3="-246.4kJ·" mol -1。 =1.86<400,反应未达到平衡状态,向正反应方向移动,故
=1.86<400,反应未达到平衡状态,向正反应方向移动,故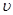 正>
正>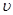 逆;设平衡时生成物的浓度为0.6+x,则甲醇的浓度为(0.44-2x)有:400=
逆;设平衡时生成物的浓度为0.6+x,则甲醇的浓度为(0.44-2x)有:400=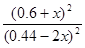 ,解得x=0.2 mol·L-1,故0.44 mol·L-1-2x=0.04 mol·L-1。
,解得x=0.2 mol·L-1,故0.44 mol·L-1-2x=0.04 mol·L-1。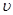 (CH3OH)="0.16" mol·L-1·min-1。
(CH3OH)="0.16" mol·L-1·min-1。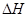 ﹥0。
﹥0。

科目:高中化学 来源:不详 题型:填空题
 Fe(固)+CO2(气) △H﹤0。已知1100℃时,K=0.263。化学平衡常数只与温度有关,不随浓度和压强的变化而变化。
Fe(固)+CO2(气) △H﹤0。已知1100℃时,K=0.263。化学平衡常数只与温度有关,不随浓度和压强的变化而变化。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
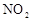 和
和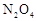 可以相互转化:
可以相互转化: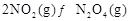 △H<0。现将一定量
△H<0。现将一定量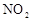 和
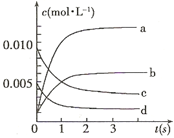
和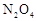 的混合气体通入一个体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图。
的混合气体通入一个体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图。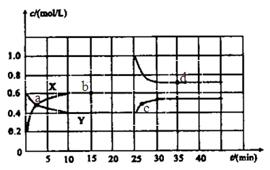
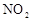 浓度随时间的变化;若在实现X、Y两条曲线变化过程中,共吸收
浓度随时间的变化;若在实现X、Y两条曲线变化过程中,共吸收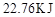 的热量,则该反应的热化学方程式为__________。
的热量,则该反应的热化学方程式为__________。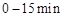 ,反应
,反应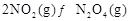 的平衡常数K(b)=__________;比较
的平衡常数K(b)=__________;比较 在
在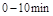 时平均反应速率
时平均反应速率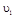 与
与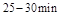 时平均反应速率
时平均反应速率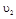 的大小__________。
的大小__________。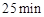 时,若只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是________(用文字表达);其平衡常数K(d)_______K(b)(填“>”、“=”或“<”)。
时,若只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是________(用文字表达);其平衡常数K(d)_______K(b)(填“>”、“=”或“<”)。 的体积百分含量与d点相同的化学平衡状态,在
的体积百分含量与d点相同的化学平衡状态,在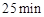 时还可以采取的措施是___________。
时还可以采取的措施是___________。| A.加入催化剂 | B.缩小容器体积 | C.升高温度 | D.加入一定量的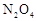 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
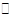 2NO+O2,达到平衡的标志是
2NO+O2,达到平衡的标志是| A.①③⑤⑥ | B.②③⑤ |
| C.①③④ | D.①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
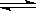 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
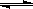 2SO3 达到平衡后,通入
2SO3 达到平衡后,通入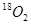 一定时间后,
一定时间后,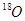 存在于( )
存在于( )| A.SO3、O2 | B.SO2、SO3 | C.SO2、O2 | D.SO2、SO3、O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是( )
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是( )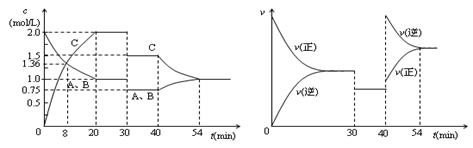
| A.8min前A的平均反应速率为0.08mol/(L·s) |
| B.30min时扩大容器的体积,40min时升高温度 |
| C.反应方程式中的x=1,正反应为吸热反应 |
| D.30min和54min的反应的平衡常数相等4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.HCl最快 | B.H2SO4最快 |
| C.CH3COOH最快 | D.一样快 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(气)+NO(气)△H<0,达到平衡后,只改变其中一个条件,对平衡的影响是:
CO2(气)+NO(气)△H<0,达到平衡后,只改变其中一个条件,对平衡的影响是:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com