
【题目】北京奥运会主体育场——“鸟巢”,被《泰晤士报》评为全球“最强悍”工程,“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料,有关说法正确的是
A.ETFE膜![]() 是由两种单体缩聚而成的
是由两种单体缩聚而成的
B.已知Ga处于ⅢA族,可推知氮化镓化学式为Ga3N2
C.合金的熔点通常比组分金属高,硬度比组分金属小
D.用金属铝与V2O5冶炼钒,铝作还原剂
科目:高中化学 来源: 题型:
【题目】利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2。下列说法正确的是

A. a为直流电源的负极
B. 阴极的电极反应式为2HSO3-+2H++e-=S2O42-+2H2O
C. 阳极的电极反应式为SO2+2H2O-2e-=SO42-+4H+
D. 电解时,H+由阴极室通过阳离子交换膜到阳极室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:P-P:198kJ·mol-1,P-O:360 kJ·mol-1,O=O:498kJ·mol-1,则反应P4(白磷)与O2反应生成P4O6的热化学反应方程式为____。

(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式_____。
(3)化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。
2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)对于反应:2NO(g)+O2(g)![]() 2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线如图:
2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线如图:


①比较p1、p2的大小关系:________。
②随温度升高,该反应平衡常数变化的趋势是________(“增大”或“减小”)。
(2)在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
①反应的ΔH______0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为__________________;平衡时混合气体中NO2的体积分数为_______。
②100℃时达平衡后,向容器中迅速充入含0.08mol的NO2和0.08mol N2O4 的混合气体,此时速率关系v(正)____v(逆)。(填“大于”,“等于”,或“小于”)
③100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。
a.T________100℃(填“大于”或“小于”),判断理由是____________________
b.列式计算温度T时反应的平衡常数K2(写计算过程):______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香花石由前20号元素中的6种组成,其化学式为![]() ,X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是
,X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是
A.原子半径:![]()
B.气态氢化物的稳定性:![]()
C.最高价氧化物对应的水化物碱性:![]()
D.![]() 、
、![]() 两化合物中R的化合价相同
两化合物中R的化合价相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.![]() 在常温下即可进行,说明正反应是放热反应
在常温下即可进行,说明正反应是放热反应
B.汽车尾气催化净化时的反应:![]()
![]() ,平衡常数为
,平衡常数为![]() ;若反应在绝热容器中进行,平衡常数为
;若反应在绝热容器中进行,平衡常数为![]() ;则
;则![]()
C.某恒容密闭容器中反应:![]()
![]() 已达平衡,则升温时
已达平衡,则升温时![]() 的值减小
的值减小
D.恒温恒容密闭容器中反应:![]() ,混合气体的密度不再改变时说明反应已达平衡
,混合气体的密度不再改变时说明反应已达平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.在固定体积的密闭容器中发生可逆反应![]() ,当混合气体的压强不再改变时,说明已达到化学平衡状态
,当混合气体的压强不再改变时,说明已达到化学平衡状态
B.对于反应![]()
![]() ,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
C.将![]() 的
的![]() 加水稀释,则溶液中
加水稀释,则溶液中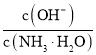 减小
减小
D.常温下向![]() 悬浊液中加入
悬浊液中加入![]() 浓溶液后,溶液中
浓溶液后,溶液中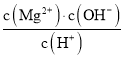 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解1升0.2mol/L的CuSO4溶液,持续通电至两极产生气体体积相等时(同条件下测定),停止电解。
(1)全过程中两极共得到的气体在标况下所占的体积___________
(2)全过程中电子转移____________摩尔
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com