
科目:高中化学 来源:2015-2016学年吉林省高二上学期第一次月考化学试卷(解析版) 题型:选择题
有体积相同、相等pH的烧碱溶液和氨水,下列叙述中正确的是
A.两溶液物质的量浓度相同
B.用同浓度的盐酸中和时,消耗盐酸的体积相同
C.两溶液中OH-离子浓度相同
D.加入等体积的水稀释后,pH仍相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期第一次月考化学试卷(解析版) 题型:选择题
在101kPa和25℃时,有关反应的热化学方程式如下:
C(s)+1/2O2(g)===CO(g)ΔH1=-110.5kJ·mol-1
H2(g)+1/2O2(g)===H2O(g)ΔH2=-241.7kJ·mol-1
H2(g)+1/2O2(g)===H2O(l)ΔH3=-285.8kJ·mol-1
下列说法正确的是
A.C(s)+H2O(g)===CO(g)+H2(g)ΔH=-131.2kJ·mol-1
B.H2燃烧热的热化学方程式为:2H2(g)+O2(g)===2H2O(l)ΔH=-571.6kJ·mol-1
C.2H2O(g)===2H2(g)+O2(g)ΔH=-483.4kJ·mol-1
D.H2O(g)===H2O(l)ΔH=-44.1kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上期中考试化学试卷(解析版) 题型:选择题
在容积相同的五个密闭容器中分别放入等量的A2和B2,在不同温度下同时任其发生反应:A2(g)+3B2(g)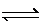 2AB3(g),分别在某一相同时刻测得其中AB3所占的体积分数变化如图所示,下列说法不正确的是
2AB3(g),分别在某一相同时刻测得其中AB3所占的体积分数变化如图所示,下列说法不正确的是
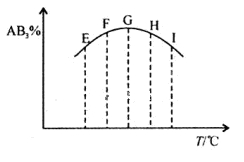
A.正反应是放热反应
B.E、F二点尚未达到平衡
C.H、I二点尚未达到平衡
D.G、H、I三点已达平衡状态
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上期中考试化学试卷(解析版) 题型:选择题
下列除去杂质的方法正确的是
A.除去N2中的少量O2:通过灼热的铜网,收集气体
B.除去CO2中的少量HCl:通入饱和Na2CO3溶液,收集气体
C.除去CO2中的少量CO:用点燃的方法
D.除去NaCl溶液中的少量MgCl2:加入适量KOH溶液,过滤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上第一次月考化学试卷(解析版) 题型:推断题
(10分)现有失去标签的四瓶无色溶液分别为Na2CO3溶液、稀盐酸、Ba(OH)2溶液、NaHSO4溶液,为确定四瓶溶液分别是什么,将其随意标号为A、B、C、D,分别取少量溶液两两混合,产生的现象如下表所示。
实验顺序 | 实验内容 | 实验现象 |
① | A + B | 生成白色沉淀 |
② | A + C | 放出无色气体 |
③ | A + D | 放出无色气体 |
④ | B + C | 无明显变化 |
⑤ | B + D | 生成白色沉淀 |
⑥ | C + D | 无明显变化 |
已知:NaHSO4属于酸式盐,在水溶液中的电离方程式为:NaHSO4 = Na+ + H+ + SO42- 。
根据实验现象,回答下列问题:
(1)A为 ,C为 。
(2)写出下列反应的离子方程式
A + B ,A + D ,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为 ,反应后得到的溶液中含有的阴离子有 。
(4)上述没有明显变化的实验④、⑥,其中 发生了离子反应,离子方程式为 。请设计实验证明其发生了反应 。(试剂任选)
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期10月月考化学试卷(解析版) 题型:选择题
汞(熔点-39℃,沸点356℃)是制造电池、电极的重要原料,历史上曾用“灼烧辰砂法”制取汞。目前工业上制粗汞的一种流程图如下。

下列分析错误的是
A.洗涤粗汞可用5%的盐酸代替5%的硝酸
B.辰砂与氧化钙加热反应时,CaSO4为氧化产物
C.“灼烧辰砂法”过程中电子转移的方向和数目可表示为:
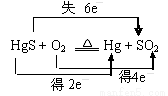
D.减压蒸馏的目的是降低汞的沸点,提高分离效率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南信阳高级中学高二开学考试化学试卷(解析版) 题型:选择题
二氟甲烷是性能优异的环保产品,它可替代某些会破坏臭氧层的“氟里昂”产品,用作空调、冰箱和冷冻库等中的致冷剂。下列关于二氟甲烷的说法正确的
A.二氟甲烷是正四面体结构 B.二氟甲烷溶于水得F— 离子
C.二氟甲烷中两个氢原子性质相同 D.二氟甲烷是极易与O3反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆巴蜀中学高一上10月月考化学试卷(解析版) 题型:实验题
(12分)某次实验需用480mL、0.5mol/L的稀H2SO4溶液,某同学用98%的浓H2SO4(ρ=1.84g/cm3)进行配制,请回答下列问题:
(1)如果实验室有10mL、15mL、50mL量筒,最好应选用 mL的量筒来量取所需的98%的浓硫酸的体积 mL。
(2)将下列步骤中的空格内将所用仪器补充填写完整
①用20mL量筒量取所需的浓硫酸
②将烧杯中的溶液转移到仪器A中(仪器A的名称为 )
③将浓硫酸缓缓注入盛有适量仪蒸馏水的烧杯中,边加边搅拌
④将溶液冷却,恢复室温
⑤向仪器A中加入蒸馏水,在距离刻度1-2cm时,改用 加蒸馏水至刻度线
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦洗涤烧杯2-3次,洗涤液也注入仪器A中,轻轻摇动仪器A,使溶液混合均匀。
(3)实验中上述步骤的正确顺序为 (填写序号)
(4)下列操作会引起所配溶液浓度偏大的是 (填写字母)
A.量筒用蒸馏水洗涤后未干燥即用来冷却浓硫酸
B.容量瓶用蒸馏水洗净后未干燥即用来配制溶液
C.定容时,观察液面俯视刻度线
E.取用浓硫酸后,将量筒用蒸馏水洗涤并将洗涤液转移容量瓶中
F.摇匀后,液面低于刻度线,没有再加蒸馏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com