
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
���� ��1���¶����ߣ�ƽ�ⳣ�����˵��ƽ�������ƶ���
��2����С������������ı�ѹǿ�Ի�ѧƽ���ƶ���Ӱ�죻
��3����ѧƽ�ⳣ�����¶ȵĺ�����ֻ���¶��йأ�����ƽ������ʽ��ƽ�ⳣ������ƽ��ʱCO��Ũ�ȣ�
��4���Ƚ�QC��K����Դ�С�����QC��K�����ƶ���QC�TK�����ƶ���QC��K�����ƶ���
��� �⣺��1����ѧƽ�ⳣ���Ĵ�Сֻ���¶��йأ������¶ȣ�ƽ�������ȵķ����ƶ����ɱ���֪�������¶ȣ���ѧƽ�ⳣ������˵����ѧƽ�������ƶ����������Ӧ�������ȣ��ʴ�Ϊ�����ȣ�
��2��830��ʱ�������еķ�Ӧ�Ѵﵽƽ�⣮�������������������£���С�������������Ϊ��Ӧ�������������ķ�Ӧ���ı�ѹǿ��Ӱ�컯ѧƽ���ƶ���
CO2��g��+H2��g��?CO��g��+H2O��g��
��ʼʱŨ�ȣ�mol/L�� 0 0 1 1
��ʼʱŨ�ȣ�mol/L�� x x x x
��ʼʱŨ�ȣ�mol/L�� x x 1-x 1-x
���¶���ƽ�ⳣ��K=$\frac{c��CO��•c��{H}_{2}O��}{c��C{O}_{2}��•c��{H}_{2}��}$=$\frac{��1-x������1-x��}{x��x}$=1
��ã�x=0.5����ƽ��ʱCO��Ũ��Ϊ��1-0.5��mol/L=0.5mol/L���ʴ�Ϊ��0.5mol/L������
��3���� 830��ʱ���������г���1mol CO��5mol H2O����Ӧ�ﵽƽ����仯ѧƽ�ⳣ�����¶ȵĺ�����ֻ���¶��йأ��¶Ȳ���K���䣬�ʴ�Ϊ�����ڣ�
��4����1200��ʱ��K=2.6����ijʱ�̸�������CO2��H2��CO��H2O��Ũ�ȷֱ�Ϊ2mol•L-1��2mol•L-1��4mol•L-1��4mol•L-1��Ũ����=$\frac{4mol/L��4mol/L}{2mol/L��2mol/L}$=4��2.6��˵����Ӧ������У��ʴ�Ϊ���淴Ӧ����
���� ������Ҫ�����¶ȶԻ�ѧƽ�⡢��ѧƽ�ⳣ����Ӱ�죬�жϷ�Ӧ���еķ����ѶȲ�����ѧ�������ͽ�������������


 �ظ���ʦ�㲦ϵ�д�
�ظ���ʦ�㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
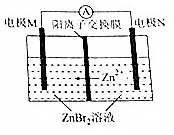 ���ܶȴ��ܵ��п������ͼ��ʾ���ŵ�ʱ�ܷ�ӦΪZnʮBr2�T-ZnBr2������˵������ȷ���ǣ�������
���ܶȴ��ܵ��п������ͼ��ʾ���ŵ�ʱ�ܷ�ӦΪZnʮBr2�T-ZnBr2������˵������ȷ���ǣ�������| A�� | �ŵ�ʱ���缫NΪ���� | |
| B�� | �ŵ�ʱ�������ĵ缫��ӦʽΪBr2+2e-�T2B- | |
| C�� | ���ʱ���缫M��ֱ����Դ�ĸ������� | |
| D�� | ���ʱ��Zn2+ͨ�����ӽ���Ĥ��������Ǩ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
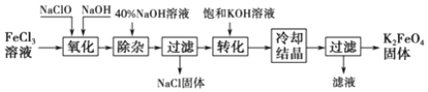
| ��ѧʽ | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
| Kaq | 8.0��10-16 | 8.0��10-18 | 8.0��10-20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
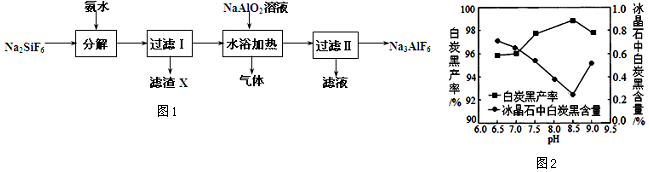
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ij��Һ�к���Fe2+���������Һ�м���ˮ���ټ����軯�� | |
| B�� | �����£�����������ʢװŨ���ᣬ������Ũ��������� | |
| C�� | Na2O2��ˮ��Ӧ��������O2������Na2O2����������������ԭ�� | |
| D�� | ����HF��ʴ����������Ϊ�����к��е�SiO2���������������ͨ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu��OH��2 ����� Cu��OH��2 �� CH3COOH | |
| B�� | BaCl2 �� Na2SO4�� Ba��OH��2 �� CuSO4 | |
| C�� | NaHCO3 �� NaHSO4�� Na2CO3 �� NaHSO4 | |
| D�� | NaHCO3�������� �� Ca��OH��2�� Ca��HCO3��2 �� NaOH�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������ٷ�����Ӧʱ��״̬ | |
| B�� | ��ϵ�е���ѹǿ����ʱ��״̬ | |
| C�� | ������Ũ����������Ũ��֮��Ϊ1��3ʱ | |
| D�� | �������ܶȱ��ֲ���ʱ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ������ | �Լ�X | ���ӷ���ʽ |
| A | ����Һ�У�Fe3+��SO42-��NO3- | ������ͭ�� | 2Fe3++Cu=2Fe2++Cu2+ |
| B | Cu2+��Al3+��AlO2-��Cl- | ���������� | AlO2-+4H++=Al3++2H2O |
| C | Na+��Ba2+��HCO3-��NO3- | NaHSO4��Һ | H++HCO3--=CO2��+H2O |
| D | pH=0����Һ�У�Mg2++��Fe2++��NO3-- | ˫��ˮ | 2Fe2++H2O2+2H+=2Fe3++2H2O |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
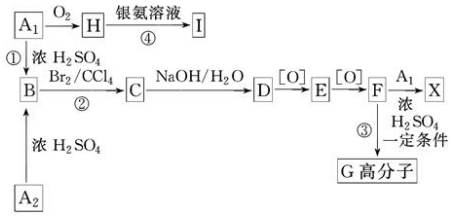
 ��
�� ��
�� ��
�� ��
��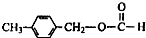
 ��
��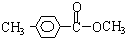 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com