

(1)电源E为__________极,F为__________极。
(2)A极的电极反应式为_______________________,析出物质__________mol。
(3)B极的电极反应式为_______________________,析出气体__________mL(标准状况)。
(4)C极的电极反应式为_______________________,析出物质__________mol。
(5)D极的电极反应式为_______________________,析出气体__________mL(标准状况)。
(6)甲烧杯中滴入石蕊试液,__________附近变红,如果继续电解,在甲烧杯中最终得到__________溶液。
解析:本题是以电解知识为依托的综合性较强的题目。由于有外接直流电源,所以装置甲、乙均为电解池,两个电解池的关系为串联。电解一段时间后,A极比C极重。故A极上必有Ag析出,由于Ag+在A级上获得电子发生了还原反应,故A极为电解池的阴极,在电解池中阴极与外接直流电源的负极相连,故E极为负极,F极为正极。根据电解池甲、乙的串联关系,可进一步得出A、B、C、D依次为阴极、阳极、阴极、阳极。电极反应依次为:A极:4Ag++4e-![]() 4Ag,B极:4OH--4e-
4Ag,B极:4OH--4e-![]() 2H2O+O2↑,C极:Cu2++2e-
2H2O+O2↑,C极:Cu2++2e-![]() Cu,D极:2Cl--2e-
Cu,D极:2Cl--2e-![]() Cl2↑,由于串联时各电极上流过的电量是相同的,假设电路中均通过4 mol电子,则A极上生成4 mol Ag,B极上生成1 mol O2,C极上生成2 mol Cu,D极上生成2 mol Cl2,这样便可得出一个关系式:4e-—4Ag—O2—2Cu—2Cl2,A极比C极重:4 mol×108 g·mol-1-2 mol×64 g·mol-1=304 g,根据A极比C极重1.9 g,可列出比例式求出反应生成的Ag和Cu的物质的量:
Cl2↑,由于串联时各电极上流过的电量是相同的,假设电路中均通过4 mol电子,则A极上生成4 mol Ag,B极上生成1 mol O2,C极上生成2 mol Cu,D极上生成2 mol Cl2,这样便可得出一个关系式:4e-—4Ag—O2—2Cu—2Cl2,A极比C极重:4 mol×108 g·mol-1-2 mol×64 g·mol-1=304 g,根据A极比C极重1.9 g,可列出比例式求出反应生成的Ag和Cu的物质的量:
n(Ag)= ![]() ×4 mol=0.025 mol,n(Cu)=0.012 5 mol,n(O2)=0.006 25 mol,n(Cl2)=0.012 5 mol。电解时甲池随着B极附近水电离产生的OH-的不断消耗,H+的物质的质量逐渐增大,所以滴入石蕊试液后B极附近变红,而A极上Ag+不断得到电子析出Ag,故在甲烧杯中最终得到HNO3溶液。
×4 mol=0.025 mol,n(Cu)=0.012 5 mol,n(O2)=0.006 25 mol,n(Cl2)=0.012 5 mol。电解时甲池随着B极附近水电离产生的OH-的不断消耗,H+的物质的质量逐渐增大,所以滴入石蕊试液后B极附近变红,而A极上Ag+不断得到电子析出Ag,故在甲烧杯中最终得到HNO3溶液。
答案:(1)负;正 (2)4Ag++4e-![]() 4Ag;0.025
4Ag;0.025
(3)4OH--4e-![]() 2H2O+O2↑;140
2H2O+O2↑;140
(4)Cu2++2e-![]() Cu;0.0125
Cu;0.0125
(5)2Cl--2e-![]() Cl2↑;280
Cl2↑;280
(6)B;HNO3


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。
⑴请根据甲同学的意图,连接相应的装置,接口顺序:
b接________,__________接 _________,_________接a。
⑵U形管中所盛试剂的化学式为_____________________________ 。
⑶装置③中CCl4的作用是___________________________________。
⑷乙同学认为甲同学实验中有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在_____________之间(填装置序号)。瓶中可以放入______________________________________。
⑸丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成__________________________,如果观察到_______________________________________的现象,则证明制Cl2时有HCl挥发出来。
查看答案和解析>>
科目:高中化学 来源:2013届辽宁省盘锦市二中高三第一次阶段考试化学试卷(带解析) 题型:实验题
(12分)金属钠与水的反应是中学化学中的一个重要反应。在高中化学教材的几次改版中该实验曾出现过几种不同的演示方法,分别如下图中甲、乙、丙所示:
(1)现按图甲所示的方法,在室温时,向盛有Ca(HCO3)2溶液的水槽中,加入一小块金属钠。下列现象描述正确的是_________(填字母)。
A.钠浮在液面上,并四处游动,最后消失
B.钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色
D.恢复到室温时,烧杯底部有固体物质析出
(2)请补充并完成甲实验中从试剂瓶中取出钠到向水槽中投入钠的有关操作:用镊子从试剂瓶中取出一小块钠→___________________________→用镊子夹取切好的金属钠投入到盛有Ca(HCO3)2溶液的烧杯中。
(3)按图乙所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列几种情况收集产生的气体在相同条件下体积最大的是( )
A.用铝箔包住钠 B.用锡箔包住钠 C.直接将钠投入的水中
(4)用装满水的矿泉水瓶按图丙方法进行实验,用手挤压矿泉水瓶共排出水的体积为112 mL,塞紧带有钠的塞子,反应结束后,干瘪的带塞矿泉水瓶恢复成原状,假设瓶内、瓶外均属于标准状况,则所用金属钠的质量是 克。
查看答案和解析>>
科目:高中化学 来源:2011届江西省南昌一中高三第一次月考化学试题 题型:实验题
(8分)为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。

⑴请根据甲同学的意图,连接相应的装置,接口顺序:
b接________,__________接 _________,_________接a。
⑵U形管中所盛试剂的化学式为_____________________________ 。
⑶装置③中CCl4的作用是___________________________________。
⑷乙同学认为甲同学实验中有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在_____________之间(填装置序号)。瓶中可以放入______________________________________。
⑸丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成__________________________,如果观察到_______________________________________的现象,则证明制Cl2时有HCl挥发出来。
查看答案和解析>>
科目:高中化学 来源:2014届江西省吉安市高一下学期期末教学质量评价化学试卷(解析版) 题型:实验题
为了研究外界条件对H2O2分解速率的影响,某同学做了以下实验,请回答下列问题。
|
编号 |
操作 |
实验现象 |
|
① |
分别在试管A、B中加入5mL 5%H2O2溶液,各滴入2滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中。 |
试管A中产生气泡量减少;试管B中产生的气泡量增大。 |
|
② |
另取两支试管分别加入5mL 5%H2O2溶液和5mL 10%H2O2溶液 |
试管A、B中均未明显见到有气泡产生。 |
(1)过氧化氢分解的化学方程式为________。
(2)实验①的目的是________。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是_______(用实验中所提供的几种试剂)。
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,则A、B、C三点所表示的瞬时反应速率最快的是______(填“A”或“B”或“C”)。

(5)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
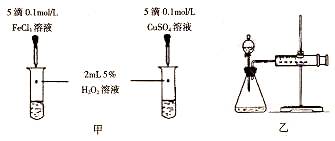
①定性分析:如图甲可通过观察_________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______。
②定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com