
下表是元素周期表的一部分,请参照①~⑥在表中的位置,用化学用语回答下列问题:
| I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ |
(1) ⑥有两种同位素,其中一种原子核内有18个中子,其原子符号为_______;
(2)②与④可以形成一种温室气体,其电子式为_______;
(3) ③和⑤的氢化物沸点 __________(填分子式)高,原因是______________;
(4)②和⑥按原子个数比为1:4形成的化合物为_______分子(填极性或非极性),含有_______键(填极性或非极性)
(5) ②形成的单质可以是不同类型的晶体,它们可能是____________(填字母)
A原子晶体 B分子晶体 C金属晶体 D离子晶体 E混合型晶体
科目:高中化学 来源: 题型:
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(杂质中不含铁元素,且杂质不与H2、H2SO4反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
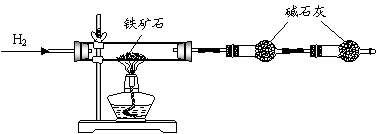 Ⅰ.铁矿石中含氧量的测定
Ⅰ.铁矿石中含氧量的测定
|
实验结果:将5.0g铁矿石放入硬质玻璃管中完全反应, 测得装置B增重1.35 g。
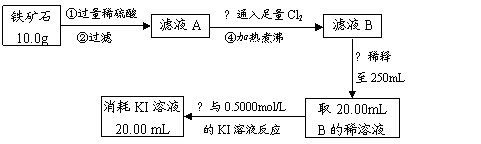 Ⅱ.铁矿石中含铁量的测定
Ⅱ.铁矿石中含铁量的测定
Ⅲ.问题讨论与解决:
(1)如要验证滤液A中铁元素的存在形式,可另取两份滤液A分别进行实验,实验方法、现象与结论如下表。请将其补充完整。
可供选择的试剂有:酸性KMnO4溶液、NaOH溶液、KSCN溶液、氯水
| 实验方法 | 实验现象 | 结论 |
| 步骤1:在滤液A中加入 ▲ | ▲ | 滤液A中有Fe3+ |
| 步骤2:在滤液A中加入 ▲ | ▲ | 滤液A中有Fe2+ |
(2)步骤④中煮沸的作用是: ▲ ;
(3)步骤③中反应的离子方程式为: ▲ ;
(4)请通过实验Ⅰ、Ⅱ计算出该铁矿石中铁的氧化物的化学式。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
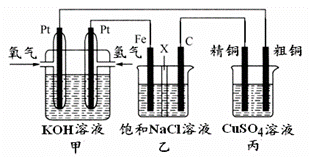
根据要求回答相关问题:
(1)通入氢气的电极为 (填“正极”或“负极”),负极的电极反应式为 。
(2)石墨电极为 (填“阳极”或“阴极”), 乙装置中阳极的电极反应式为_____________。
(3)反应一段时间后,在乙装置中滴入酚酞溶液, _ 区(填“铁极”或“石墨极”)的溶液先变红。
(4)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将 (填“增大”“减
小”或“不变”)。
(5)若在标准状况下,有224m L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为 ;丙装置中阴极析出铜的质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
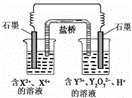
右下图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是
A.左池电极反应式:X4+ + 2e-=X2+
B.每消耗1mol Y2O72-,转移3mol电子
C.改变右池溶液的c(H+),电流强度不变
D.左池中阴离子数目增加
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.共价键的键能越大,分子晶体的熔点越高
B.失去电子难的原子获得电子的能力一定强
C.在化学反应中,某元素由化合态变为游离态,则该元素一定被还原
D.电子层结构相同的不同简单离子,其半径随核电荷数增多而减小
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C三种短周期元素在周期表中的位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则下列说法正确的组合是
| A | B |
| C |
①B、C形成的单质均存在同素异形体
②X的种类比Y多
③常温下,B的氢化物不能电离出H+
④C的最高价氧化物对应的水化物是强酸( )
A.①②③④ B.②④ C.①② D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学用语的表示正确的是
A.质子数为35、中子数为45的溴原子: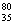 Br
Br
B.过氧化钠的电子式:
C.硫离子的结构示意图: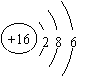

D.苯的结构简式:C6H6
查看答案和解析>>
科目:高中化学 来源: 题型:
a~e是元素周期表中前四周期元素,请根据表中信息回答下列问题:

⑴a在周期表中的位置为________________________
⑵b的基态原子中,有电子运动的原子轨道有____个,
核外电子按能量不同可分为_____种,
⑶用小黑点在图中标出b、c及其同周期相邻元素的第一电离能的相对位置,注明相应的元素符号(图中黑点为电负性最大的c)。
⑷配合物甲由e3+与水分子、元素d构成,已知该配合物中e3+的配位数为6。在含有0.1mol甲的溶液中加入AgNO3溶液至过量,经过滤、洗涤、干燥后,得到28.7g白色沉淀。则甲的电离方程式为____________________________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com