
(6分)用溴置换碘的反应式为:Br2 + 2 I- = 2 Br- + I2 ;用碘置换溴的反应式为:
I2 + 2 BrO3- = 2 IO3- + Br2。两个置换反应矛盾吗?简述理由。
科目:高中化学 来源: 题型:
| .. | ||
|
| .. | ||
|
| .. | ||
|
| .. | ||
|
查看答案和解析>>
科目:高中化学 来源: 题型:
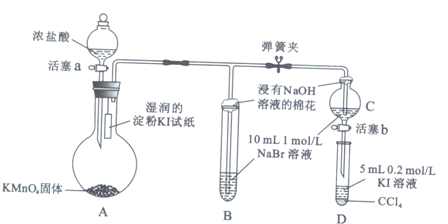
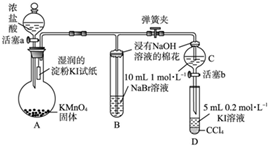 为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)
为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)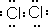
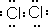
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com