
【题目】下图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。

图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液。
(1)在上述装置中,实验时需要加热的仪器为(填仪器或某部位的代号) _____________________。
(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是_____________。
(3)检验乙醇氧化产物时F中的实验现象是____________________________。
(4)E处是一种纯净物,其反应方程式为_______________________________________。
(5)写出乙醇发生催化氧化的化学方程式_______________________________________。
【答案】 E A B F 水浴加热 有砖红色沉淀生成 2KMnO4 ![]() K2MnO4+ MnO2+O2↑ 2CH3CH2OH + O2
K2MnO4+ MnO2+O2↑ 2CH3CH2OH + O2 ![]() 2CH3CHO + 2H2O
2CH3CHO + 2H2O
【解析】(1)固体加热制氧气需要加热,乙醇变为蒸汽需加热,乙醇的催化氧化要加热,醛和氧气的反应也要加热,故答案为:E、A、B、F;
(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是水浴加热;故答案为:水浴加热;
(3)乙醛能和氢氧化铜悬浊液反应,生成砖红色沉淀,所以F中会产生红色沉淀,故答案为:F中产生红色沉淀;
(4)固体纯净物加热制氧气的只能是加热高锰酸钾制氧气,反应为:2KMnO4![]() K2MnO4+MnO2+O2↑,故答案为:2KMnO4
K2MnO4+MnO2+O2↑,故答案为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(5)乙醇发生催化氧化的化学方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。


科目:高中化学 来源: 题型:
【题目】2016年冬季,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
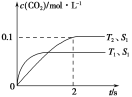
据此判断:
①该反应的ΔH________0(填“>”或“<”)。
②在T2温度下,0~2 s内的平均反应速率v(N2)________。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填代号)。
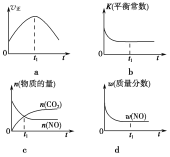
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:
CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ΔH1=-867 kJ/mol
2NO2(g) ![]() N2O4(g) ΔH2=-56.9 kJ/mol
N2O4(g) ΔH2=-56.9 kJ/mol
写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式:_______________________
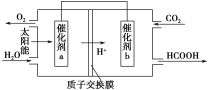
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂b表面发生的电极反应式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】EHPB是合成治疗高血压和充血性心力衰竭的药物的中间体,合成路线如下:
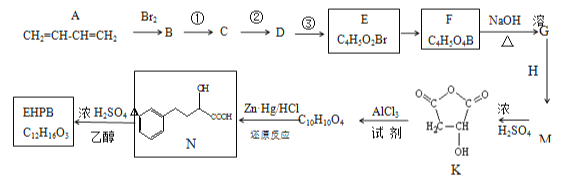
已知:ⅰ.碳碳双键容易被氧化
ⅱ. ![]()
(1)A的名称为______,E中含氧官能团的名称为_______。
(2)E由B经①、②、③合成。
a.①的反应试剂和条件是__。 b.③ 的反应类型是______。
(3)M的结构简式为__________。
(4)EHPB不能与NaHCO3反应,写出有机物N→EHPB的化学方程式为_____________。
(5)有机物N有多种同分异构体,其中能满足下列条件的同分异构体有_________种。
a.含有酚羟基 b.能发生水解反应且能发生银镜反应c.苯环上的一氯代物只有一种 d.核磁共振氢谱有5组峰
(6)请写出由苯和乙二醇制取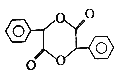 的转化过程________,无机试剂任选。
的转化过程________,无机试剂任选。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的体积和所得沉淀的物质的量的关系如下图所示(b处NaOH的体积为1L),则下列判断错误的是 ( )

A. NaOH的浓度为0.6 mol·L-1 B. 在a点处溶液中的溶质为NaCl
C. 混合溶液中n(Al3+)﹕n(Mg2+)=1﹕1 D. 图中线段oa : ab=4﹕1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 活化分子相互碰撞即可发生化学反应
B. 升高温度会加快化学反应速率,其原因是增加了活化分子的百分率
C. 某一反应的活化分子百分率是个定值
D. 浓度增大使得反应物分子中的活化分子百分率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物完全燃烧生成标准状况下CO2的体积为4.48 L,H2O的质量为5.4 g ,
(1)若此有机物的质量为3 g,则此有机物的结构简式是_________________________;
(2)若此有机物的质量为4.6 g,则此有机物的分子式是________________________;
(3)若此有机物的质量为6.2 g,且此有机物1mol能和金属钠反应生成1 mol H2,则此有机物的结构简式是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A. 铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑
B. 过氧化钠与反应:2O22-+2H2O=4OH-+O2↑
C. 碳酸氢钠与稀盐酸反应:CO32-+2H+=CO2↑+ H2O
D. 氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-=Fe(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅单质及其化合物的说法正确的是( ) ①硅是构成一些岩石和矿物的基本元素
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷是人类应用很早的硅酸盐材料.
A.①②
B.②③
C.①④
D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。利用方铅矿精矿( PbS)直接制备硫酸铅粉末的流程如下:

已知:(i) PbCl2 (s)+2C1-(aq)=PbCl42-(aq) △H>0
(ii)有关物质的Ksp和沉淀时的pH如下:
物质 | Ksp | 物质 | 开始沉淀时pH | 完全沉淀时pH |
PbSO4 | 1.0×10-8 | Fe(OH)3 | 2.7 | 3.7 |
PbCl2 | 1.6×10-5 | Pb(OH)2 | 6 | 7.04 |
(1)步骤I反应加入盐酸后可以观察到淡黄色沉淀生成,请写出的离子方程式___________。
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因____________。
(3)在上述生产过程中可以循环利用的物质有______________。
(4)写出步骤Ⅲ中PbCl2晶体转化为PbSO4沉淀的离子方程式________________。
(5)铅的冶炼、加工会使水体中重金属铅的含量增大造成严重污染。某课题组制备了一种新型脱铅剂(用EH表示),能有效去除水中的痕量铅,脱铅过程中主要发生的反应为:2EH(s)+Pb2+![]() E2Pb(s)+2H+。则脱铅的最合适的pH范围为____(填编号)
E2Pb(s)+2H+。则脱铅的最合适的pH范围为____(填编号)
A.4~5 B.6~7 C.9~10 D.11~12
(6)PbSO4热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl-KC1混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。

①放电过程中,Li+向_______移动(填“负极”或“正极”)。
②负极反应式为_____________。
③电路中每转移0.2mol电子,理论上生成_________g Pb。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com