
在一定温度下,有A.盐酸 b.硫酸 c.醋酸三种酸,下列说法正确的是( )
A.等物质的量浓度的三种酸的pH由大到小的关系为b>a>c
B.等物质的量浓度等体积的三种酸,与等浓度的NaOH溶液反应,消耗碱的体积 由大到小的顺序是a=b=c
由大到小的顺序是a=b=c
C.三者pH相同、体积相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是c>a=b
D.三者pH相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则三者的初始反应速率大小关系为b >a>c
科目:高中化学 来源:2016-2017学年辽宁师大附中高二12月月考化学试卷(解析版) 题型:选择题
进行一氯取代反应后,只能生成三种沸点不同产物的烷烃是( )
A.(CH3)2CHCH2CH2CH3 B.(CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2 D.(CH3)3CCH2CH3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上第二次考试化学卷(解析版) 题型:填空题
取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如下图所示,试回 答下列问题:
答下列问题:
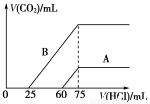
(1)原NaOH溶液的物质的量浓度为____________mol/L。
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是____________,其物质的量之比为__________。
(3)曲线B表明,所得溶液加盐酸后产生CO2气体体积(标况)的最大值为 mL。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上第二次考试化学卷(解析版) 题型:选择题
已知在碱性溶液中可发生如下反应:Fe(OH)3+ClO-+OH-→FeO4n-+Cl-+ H2O(未配平)。则有关叙述不正确的是
H2O(未配平)。则有关叙述不正确的是
A.已知FeO4n-中Fe的化合价是+6价,则n=2
B.每产生1molCl-,转移2mol电子
C.若n=2,该反应中氧化剂与还原剂的物质的量之比为2:3
D.FeO4n-具有强氧化性,一般其还原产物为Fe3+,可用作新型自来水消毒剂和净水剂
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第二次考试化学卷(解析版) 题型:填空题
( 14分)
I .(1)已知H2的燃烧热285.8KJ/mol,写出液态水电解生成H2和O2的热化学方程式 ;
(2)已知2SO2(g)+O2(g) = 2SO3(g) ΔH=-197 kJ/mol,相同温度和压强条件下,4molSO2和2molO2充入容器中反应至平衡时放出的能量为Q KJ,则Q 394KJ(填“>”“<”或“=”)
II.甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g) CH3OH
CH3OH (g)+H2O(g) ΔH1
(g)+H2O(g) ΔH1
反应II:CO(g)+2H2(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
(1)由表中数据判断ΔH2 0(填“>”、“<”或“=”),
(2)若容器容积不变,下列措施可增加甲醇产率的是 ,
A.升高温度
B.将CH3OH(g)从体系中分离
C.使用合适的催化剂
D.恒温恒容充入He,使体系总压强增大
E.按原比例再充入 CO和 H2
(3)某温度下,将2 mol CO和6 mol H2充入2L的恒容密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为 ,此时的温度为 (从上表中选择);
(4)恒温下,1mol CO和nmol H2在一个容积可变的密闭容器中反应达到平衡后,生成a molCH3OH.若起始时放入3molCO+3nmolH2,则达平衡时生成CH3OH_______mol。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第二次考试化学卷(解析版) 题型:选择题
常温条件,下列溶液的有关说法正确的是( )
A.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,C(H+)= C(OH-)
B.pH=a的氨水溶液,稀释10倍后,其pH=a -1
C.0.1mol/L的稀硫酸和0.1mol/L氨水等体积混合后:c(NH4+)+c(NH3·H2O) = c(SO42-)
c(SO42-)
D.向CH3COONa溶液中通入少量HCl气体,溶液的pH增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上月考三化学卷(解析版) 题型:填空题
合金贮氢材料具有优异的吸放氢性能,在配合氢能的开发中起 到重要作用。
到重要作用。
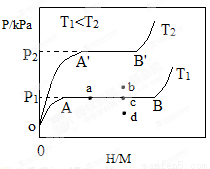
(1)一定温度下,某贮氢 合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐惭增大;在AB段,MH与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)
合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐惭增大;在AB段,MH与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g) zMHy(s) △H1(I);B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。
zMHy(s) △H1(I);B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。
反应(I)的焓变△HⅠ_______0(填“>”“<”或“=”)。
反应(I)中z=___________(用含x和y的代数式表示)。
温度为T1时,2g某合金4min内吸收氢气240mL,吸氢速率v=________mL•g?1•min?1。
(2)当反应(I)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡后反应(I)可能处于图中的_______点(填“b”“c”或“d”),该贮氢合金可通过______或_______的 方式释放氢气。η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)___ _______η(T2)(填“>”“<”或“=”)。
方式释放氢气。η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)___ _______η(T2)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上月考三化学卷(解析版) 题型:选择题
有机物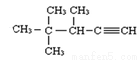 的名称为
的名称为
A.2,2,3-三甲基-1-戊炔 B.3,4,4-三甲基-l-戊炔
C.3,4,4-三甲基辛炔 D.2,2,3-三甲基-4-戊炔
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江牡丹江第一高级中学高三12月月考化学卷(解析版) 题型:选择题
某硫酸厂废气中SO2的回收利用方案如下图所示,下列说法不正确的是

A.X可能含有2种盐 B.a是SO3
C.Y中含有(NH4)2SO4 D.(NH4)2S2O8中S的化合价不可能为+7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com