
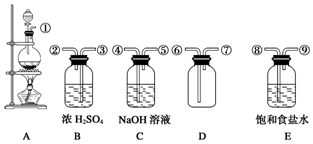
分析 跟据实验的目的和反应的原理可知,实验室用二氧化锰和浓盐酸在A装置制备氯气,制得的氯气中混有氯化氢气体和水蒸气,分别通入盛有饱和氯化钠溶液的洗气瓶和盛有浓硫酸的洗气瓶,除杂干燥后用向上排空法收集氯气,氯气有毒,不能直接排放到空气中,应用盛有NaOH溶液的装置吸收氯气,反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O,据此分析解答.
解答 解:(1)装置A为二氧化锰与浓盐酸制备氯气的反应,化学方程式为:MnO2+4HCl (浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2;
故答案为:MnO2+4HCl (浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2;
(2)由分析可知,A装置制备的氯气含有氯化氢气体和水蒸气,故用盛放饱和食盐水的装置E除氯化氢,和盛放浓硫酸的装置B吸收水,在D中收集干燥的氯气,氯气有毒,最后用盛放氢氧化钠的装置C吸收;
故答案为:A;E;B;D;C;
(3)B瓶中浓H2SO4的作用是干燥氯气,E瓶盛有的饱和食盐水的作用是除氯化氢气体;
故答案为:干燥氯气;除氯化氢气体;
(4)氯气有毒,C瓶中盛有NaOH溶液是为了尾气处理,吸收多余的氯气,发生的反应为:Cl2+2NaOH=NaCl+NaClO+H2O;
故答案为:尾气处理,吸收多余的氯气;Cl2+2NaOH=NaCl+NaClO+H2O.
点评 本题考查较为综合,题目难度不大,注意实验室制备气体的实验装置和反应原理,把握物质的主要性质,会根据实验目的选取合适的装置和试剂.


科目:高中化学 来源: 题型:多选题
| A. | 向某溶液中加入BaCl2溶液,产生白色沉淀,再加盐酸,沉淀不溶解,该溶液一定含有SO42- | |
| B. | 向某溶液中同时加入几滴KSCN溶液和少量新制氯水,溶液变为红色,该溶液一定含有Fe2+ | |
| C. | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体,该溶液不一定含有CO32- | |
| D. | 向某溶液中加入稀硝酸后,再加入AgNO3溶液,产生白色沉淀,则该溶液中含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③⑤ | C. | ③⑥⑦ | D. | ⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2 加氢合成甲醇是合理利用CO2的有效途径.由CO2制备甲醇过程可能涉及反应如下:
甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2 加氢合成甲醇是合理利用CO2的有效途径.由CO2制备甲醇过程可能涉及反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)2═Ca2++2OH- | B. | KNO3═K++NO3- | ||
| C. | H2SO4═2H++SO42- | D. | Na2SO3═Na2++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
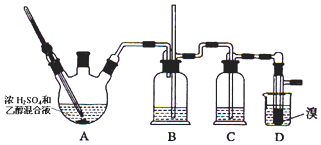
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132[ | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 形成离子键的阴阳离子键只存在静电吸引力 | |
| B. | HF、HCl、HBr、HI的还原性从左到右依次减弱 | |
| C. | ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 | |
| D. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素A、B组成的化合物常温下一定呈气态 | |
| B. | 工业上常用电解法制备元素C、D、E的单质 | |
| C. | 常温下,元素B、D的最高价氧化物对应的水化物之间能发生反应 | |
| D. | 化合物AE与CE具有相同类型的化学键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com