
³£ĪĀŹ±£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
| A£®pH=9µÄNH4ClÓėNH3”¤H2O»ģŗĻČÜŅŗÖŠc(Cl-)>c(NH4+) |
| B£®pH=2.5µÄæÉĄÖÖŠc£ØH+£©ŹĒpH=3.5µÄÄūĆŹĖ®ÖŠc£ØH+£©µÄ1 0±¶ |
| C£®AgClŌŚ0.1 mol£ÆL CaCl2ČÜŅŗŗĶ0.l mol£ÆL NaClČÜŅŗÖŠµÄČܽā¶ČĻąĶ¬ |
| D£®1 mL l mol l L Na2CO3ČÜŅŗ¼ÓĖ®Ļ”ŹĶÖĮ100 mL£¬pHŗĶKw¾ł¼õŠ” |
B
½āĪöŹŌĢā·ÖĪö£ŗA”¢pH=9µÄNH4ClÓėNH3”¤H2O»ģŗĻČÜŅŗÖŠNH3”¤H2OµÄµēĄė³Ģ¶Č“óÓŚNH4ClµÄĖ®½ā³Ģ¶Č£¬ĖłŅŌc(Cl-)<c(NH4+)£¬“ķĪó£»B”¢pH=2.5µÄæÉĄÖÖŠc£ØH+£©=1”Į10-2.5mol/L£¬pH=3.5µÄÄūĆŹĖ®ÖŠc£ØH+£©=1”Į10-3.5mol/L£¬Ē°ÕߏĒŗóÕßµÄ10±¶£¬ÕżČ·£»C”¢0.1 mol£ÆL CaCl2ČÜŅŗŗĶ0.l mol£ÆL NaClČÜŅŗÖŠµÄĀČĄė×ÓµÄÅØ¶Č²»Ķ¬£¬µ¼ÖĀAgClµÄČܽā¶Č²»Ķ¬£¬“ķĪó£»D”¢KwŹĒĪĀ¶Č³£Źż£¬ĪĀ¶Č²»±ä£¬Kw²»±ä£¬“ķĪ󣬓š°øŃ”B”£
æ¼µć£ŗæ¼²é»ģŗĻŅŗµÄĄė×ÓÅØ¶ČµÄ±Č½Ļ£¬pHµÄ¼ĘĖć£¬ČÜŅŗĻ”ŹĶ¹ż³ĢÖŠpHŗĶKwµÄÅŠ¶Ļ£¬Ķ¬Ņ»ĪļÖŹŌŚ²»Ķ¬ČܼĮÖŠµÄČܽā¶ČµÄÅŠ¶Ļ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
³£ĪĀĻĀÓŠA”¢B”¢C”¢D·Ö±šŹĒCH3COONa”¢NH4Cl”¢Na2SO4ŗĶŃĪĖįĖÄÖÖČÜŅŗÖŠµÄŅ»ÖÖ£¬ŅŃÖŖA”¢BČÜŅŗµÄpHĻąĶ¬£¬A”¢CČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČĻąĶ¬£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£® BČÜŅŗµÄpH<7 £¬DČÜŅŗµÄpH>7
B£® BČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č×ī“ó
C£® CÓėDµČĢå»ż»ģŗĻŗó£¬ČÜŅŗÖŠc(OH-)=c(CH3COOH)+ c(H£«)
D£® AÓėBµČĢå»ż»ģŗĻŗó£¬ČÜŅŗÖŠc(NH4+)> c(Cl-)> c(H+) > c(OH-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
³£ĪĀĻĀ£¬ĻĀĮŠÓŠ¹ŲĪļÖŹµÄĮæÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ£Ø £©
| A£®µČĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗÖŠ£¬Ė®µēĄė³öµÄc£ØH+£©£ŗHCl£¾CH3COOH |
| B£®pHĻąĶ¬µÄČÜŅŗÖŠ£ŗc£ØNa2CO3£©£¼c£ØNaHCO3£© |
| C£®ŌŚNa2SO3ČÜŅŗÖŠ£ŗc£ØNa+£©= 2c£ØSO32-£©+ c£ØHSO3-£©+ c£ØOH-£© |
| D£®0.1mol”¤L-1NaHSČÜŅŗÖŠ£ŗc£ØNa+£©= c£ØHS££© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖĖ®ŌŚ25”ęŗĶ95”ꏱ£¬ĘäµēĄėĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø“ķĪóµÄ
| A£®AĒśĻß“ś±ķ25”ꏱĖ®µÄµēĄėĘ½ŗāĒśĻß |
| B£®µ±95”ꏱ£¬pH=6µÄČÜŅŗ³ŹÖŠŠŌ |
| C£®25”ꏱ£¬½«10mLpH=12µÄNaOHČÜŅŗÓė1mLpH=1µÄH2SO4 ČÜŅŗ»ģŗĻ£¬ĖłµĆČÜŅŗµÄpH=7 |
| D£®95”ꏱ£¬µČĢå»żµČĪļÖŹµÄĮæÅØ¶ČµÄHAČÜŅŗŗĶNaOHČÜŅŗ»ģŗĻŗ󣬵±»ģŗĻČÜŅŗµÄpH=6Ź±£¬ĖµĆ÷HAĖįĪŖČõĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
³£ĪĀĻĀ£¬Ļņ20.00 mL 0.1000 mol”¤L£1CH3COONaČÜŅŗÖŠÖšµĪ¼ÓČė0.1000 mol”¤L£1ŃĪĖį£¬»ģŗĻČÜŅŗµÄpHÓėĖł¼ÓŃĪĖįĢå»żµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ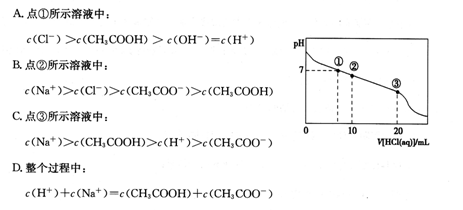
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
³£ĪĀĻĀ£¬Ļņ20.00 mL 0.100 mol”¤L£1 CH3COONaČÜŅŗÖŠÖšµĪ¼ÓČė0.100 0 mol”¤L£1ŃĪĖį£¬ČÜŅŗµÄpHÓėĖł¼ÓŃĪĖįĢå»żµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾(²»æ¼ĀĒ»Ó·¢)”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
| A£®µć¢ŁĖłŹ¾ČÜŅŗÖŠ£ŗc(CH3COOH)£½c(Cl£)£¾c(OH£)£½c(H£«) |
| B£®µć¢ŚĖłŹ¾ČÜŅŗÖŠ£ŗc(Na£«)£¾c(Cl£)£¾c(CH3COO£)£¾c(CH3COOH) |
| C£®µć¢ŪĖłŹ¾ČÜŅŗÖŠ£ŗc(CH3COOH)£¾c(Na£«)£¾c(H£«)£¾c(CH3COO£) |
| D£®Õūøö¹ż³ĢÖŠæÉÄܳöĻÖ£ŗc(H£«)£«c(Na£«)£½c(CH3COOH)£«c(CH3COO£) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
³£ĪĀĻĀ£¬ĻĀĮŠø÷×éĄė×ÓŌŚÖø¶ØČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ
A£®µĪČė·ÓĢŖČÜŅŗĻŌŗģÉ«µÄČÜŅŗÖŠ£ŗK£«”¢Na£«”¢Cu2£«”¢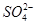 |
B£®¼ÓČė¹żĮæNaOHČÜŅŗ»ņÉŁĮæĻ”H2SO4Ź±£¬¶¼ÄܲśÉś°×É«³ĮµķµÄČÜŅŗ£ŗAl3£«”¢Ba2£«”¢Cl£”¢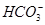 |
C£®Ė®µēĄė²śÉśµÄc(H£«)£½10£13mol”¤L£1µÄČÜŅŗÖŠ£ŗNa£«”¢Cl£”¢ ”¢ ”¢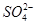 |
D£®0.1 mol”¤L£1HNO3ČÜŅŗÖŠ£ŗMg2£«”¢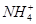 ”¢Fe2£«”¢Cl£ ”¢Fe2£«”¢Cl£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
³£ĪĀĻĀ£¬ÅØ¶Č¾łĪŖ0.1 mol/L µÄĻĀĮŠĖÄÖÖŃĪČÜŅŗ£¬ĘäpH²ā¶ØČēĻĀ±ķĖłŹ¾£ŗ
| ŠņŗÅ | ¢Ł | ¢Ś | ¢Ū | ¢Ü |
| ČÜŅŗ | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 8.8 | 9.7 | 11.6 | 10.3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ČēĶ¼±ķŹ¾ČÜŅŗÖŠc(H£«)ŗĶc(OH£)µÄ¹ŲĻµ£¬ĻĀĮŠÅŠ¶Ļ“ķĪóµÄŹĒ
| A£®Į½ĢõĒśĻß¼äČĪŅāµć¾łÓŠc(H£«)”Įc(OH£)£½Kw |
| B£®MĒųÓņÄŚČĪŅāµć¾łÓŠc(H£«)£¼c(OH£) |
| C£®Ķ¼ÖŠT1£¼T2 |
| D£®XZĻßÉĻČĪŅāµć¾łÓŠpH£½7 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com