
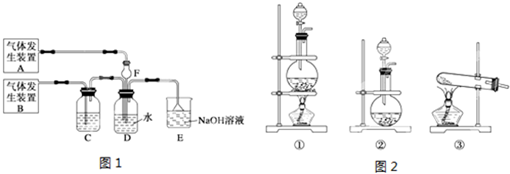
分析 (1)MnO2和浓盐酸混合加热生成氯化锰、水和氯气;
(2)气体容易与水反应,且溶解度较大会发生倒吸;根据反应原理来选择反应装置;
(3)D中是二氧化硫和氯气发生的氧化还原反应生成硫酸和盐酸,依据反应产物写出离子方程式;
(4)氯气过量可以设计实验验证氯气的氧化性,结合亚铁离子被氧化为铁离子后,加入硫氰酸钾溶液会变红色证明;二氧化硫过量可以依据二氧化硫具有漂白性设计实验和选择试剂验证.
解答 解:(1)MnO2和浓盐酸混合加热生成氯化锰、水和氯气,离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)SO2易与水反应,且溶解度较大会发生倒吸,则F可以防倒吸,装置B为制取氯气的装置,由固液反应且加热的原理可知应选择①,
故答案为:防止倒吸;①;
(3)D中是二氧化硫和氯气发生的氧化还原反应生成硫酸和盐酸,反应的离子方程式为:Cl2+SO2+2H2O═4H++2Cl-+SO42-,
故答案为:Cl2+SO2+2H2O═4H++2Cl-+SO42-;
(4)为验证通入D装置中的气体是Cl2还是SO2过量,若Cl2过量,取适量D中溶液滴加至盛有氯化亚铁溶液,试剂的试管内,再加入硫氰化钾溶液会变血红色,证明氯气氧氧化亚铁离子;若SO2过量,取适量D中溶液滴加至盛有品红溶液的试管中,红色褪去,加热又恢复红色,证明含有二氧化硫,
故答案为:②③;溶液变为红色;④;红色褪去为无色,加热后又变为红色.
点评 本题考查二氧化硫、氯气的性质,明确物质的性质及发生的化学反应是解答本题的关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 如图是镁一空气燃料电池工作原理示惫图,电池总反应为:2Mg+O2+2H2O=2Mg(OH)2.下列有关该电池的说法正确的是( )
如图是镁一空气燃料电池工作原理示惫图,电池总反应为:2Mg+O2+2H2O=2Mg(OH)2.下列有关该电池的说法正确的是( )| A. | a极为负极,发生还原反应 | |
| B. | b电极上电极反应:O2+2H2O+4e-=4OH- | |
| C. | 工作时电子由b极经外电路流向a极 | |
| D. | 该装置实现了电能转化成化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②⑤⑥ | C. | ①②④⑤ | D. | ②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O4的摩尔质量是64g | |
| B. | O4与O3、O2互为同位素 | |
| C. | 相同质量的O4与O3所含原子个数之比为1:1 | |
| D. | 32gO4所含的电子数为32NA(NA为阿伏加德罗常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| B. | 硫化钠和硫酸亚铁固体长期暴露在空气中变质 | |
| C. | 常温下铁和铂都不溶于浓硝酸 | |
| D. | H2O2溶液中加入少量MnO2或FeCl3溶液都能增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
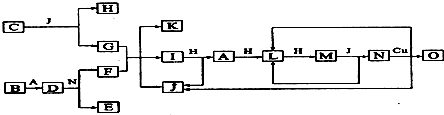
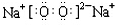 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
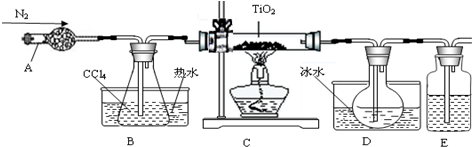
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
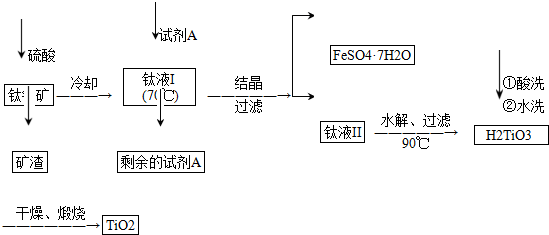
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Z |
| A. | 原子半径:r(Y)>r (Z)>r (W) | |
| B. | Y、Z、W的简单离子的电子层结构相同 | |
| C. | XWm与YWn中化学键类型相同(m、n为正整数) | |
| D. | 元素Z 的简单气态氢化物的热稳定性比W 的强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com