
在25 ℃、101 kPa条件下,将15 L O2通入10 L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复到原来的温度和压强。
(1)若剩余气体的体积是15 L,则原CO和H2的混合气体中:
V(CO)=________L, V(H2)=________L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气体中,
V(CO)∶V(H2)=________________。
(3)若剩余气体的体积为a L,则a的取值范围是___________。
科目:高中化学 来源: 题型:
元素H、C、N、O、F都是重要的非金属元素,Fe、Cu是应用非常广泛的金属。
(1)Fe元素基态原子的核外电子排布式为 。
(2)C、H元素形成的化合物分子中共有16个电子,该分子中σ键与π键的个数比为 。
(3)C、N、O三种元素的第一电离能由大到小的顺序为(用元素符号表示) 。
(4)在测定HF的相对分子质量时,实验测得值一般高于理论值,其主要原因是
。
(5)C、N两元素形成的化合物C3N4形成的原子晶体,结构类似金刚石,甚至硬度超过金刚石,其原因是
。
(6)如图为石墨晶胞结构示意图,该晶胞中含有C原子的个数为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是(NA为阿伏加德罗常数的值)( )
A.常温常压下,22.4 L CO2中含有NA个CO2分子
B.标准状况下,22.4 L空气含有NA个单质分子
C.22.4 L Cl2中含有NA个Cl2分子
D.标准状况下,1.12 L O2和1.12 L CO 2均含0.1NA个氧原子
2均含0.1NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
在反应X+2Y===R+2M中,已知R和M的摩尔质量之比为22∶9,当1.6 g X与Y完全反应后,生成4.4 g R。则在此反应中Y和M的质量之比为( )
A.16∶9 B.23∶9 C.32∶9 D.46∶9
查看答案和解析>>
科目:高中化学 来源: 题型:
在273 K和101 kPa的条件下,将2.00 g氦气、1.40 g氮气和1.60 g氧气混合,该混合气体的体积是
A.6.72 L B.7.84 L C.10.08 L D.13.44 L
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏伽德罗常数。已知C2H4和C3H6的混合物的质量为ag,则该混合物
A.所含共用电子对数目为(a/7+1)NA B.所含碳氢键数目为aNA/7
C.燃烧时消耗的O2一定是33.6a/14L D.所含原子总数为aNA/14
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是 ( )
)
A.Ba2+、NO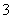 、NH
、NH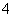 、Cl-
、Cl-
B.Ca2+、HCO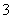 、NH
、NH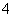 、AlO
、AlO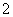
C.K+、Ba2+、Cl-、HSO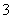
D.Mg2+、NH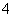 、SO
、SO 、K+
、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
Fe(OH)3胶体区别于FeCl3溶液最本质的特点是( )
A.Fe(OH)3胶体粒子的大小在1~100 nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一、稳定的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
|
| A. | 标准状况下,11.2 L乙烯含有的极性共价键数为NA |
|
| B. | 常温下,5.6 L NO和5.6 L O2的混合气体中含有的分子数为0.5NA |
|
| C. | 16.9 g BaO2固体中阴、阳离子总数为0.2NA |
|
| D. | 含有1 mol Fe(OH)3的氢氧化铁胶体中含有胶粒数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com