
电子工业常用30%的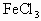 溶液腐蚀敷有铜箔的绝缘板,制成印刷线路板.这其中发生的离子方程式为________.
溶液腐蚀敷有铜箔的绝缘板,制成印刷线路板.这其中发生的离子方程式为________.
为了从使用过的废腐蚀液中回收铜,并制得纯净的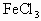 溶液,拟采用下列实验.请在各步骤的空格中填写适当的化学式以达实验目的.
溶液,拟采用下列实验.请在各步骤的空格中填写适当的化学式以达实验目的.
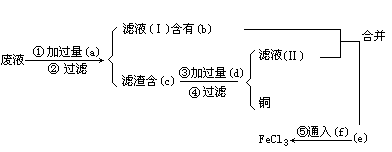
(a)________,(b)________,(c)________,(d)________,(e)________,(f)________.
科目:高中化学 来源: 题型:
 (2010?潍坊一模)铁元素及其化合物与人类的生产生活息息相关,
(2010?潍坊一模)铁元素及其化合物与人类的生产生活息息相关,| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源:2012-2013年广东陆丰碣石中学高一下学期第一次月考化学试卷(带解析) 题型:实验题
(I) 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。用FeCl3溶液做腐蚀液与Cu反应生成CuCl2和FeCl2。
(1) 写出该反应的化学方程式 。
(2) 检验溶液中Fe3+存在的试剂是 ,证明Fe3+存在的现象是 。
(Ⅱ) 印刷电路的废腐蚀液含有大量CuCl2、FeCl2、FeCl3,任意排放会造成环境污染及资源的浪费。通过下列流程可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。
⑴ 步骤①中发生反应的离子方程式 。
(2) 步骤②需加入的试剂A是 (填化学式)。
(3) 步骤③通入的气体B是 (填化学式),写出该反应的化学方程式 。
(4) 为测定滤渣中铜的质量分数,取50g的滤渣与足量的试剂A反应,得到5.6L气体(标准状况下),试计算滤渣中铜的质量分数。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年重庆市五区高三第一次学生学业调研抽测理综化学试卷(解析版) 题型:填空题
铁元素及其化合物与人类的生产生活息息相关,试回答下列问题:
(1)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,该反应的离子方程式为 。
(2)已知:Fe(s)+ O2(g)
O2(g) FeO(s)
△H=-272 kJ·mol-1
FeO(s)
△H=-272 kJ·mol-1
C(s)+O2(g) CO2(g) △H=-393.5 kJ·mol-1
CO2(g) △H=-393.5 kJ·mol-1
2C(s)+O2(g) 2CO(g) △H=-221 kJ·mol-1
2CO(g) △H=-221 kJ·mol-1
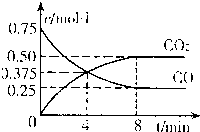
则高炉炼铁过程中
FeO(s)+CO(g) Fe(s)+CO2(g) △H=
。
Fe(s)+CO2(g) △H=
。
(3)铁红(Fe2O3)是一种红色颜料。将一定量的铁红溶于160mL 5 mol·L-1盐酸中,再加入足量铁粉,待反应结束共收集到气体2.24L(标准状况),经检测溶液中无Fe3+,则参加反应的铁粉的质量为 。
(4)以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如下图所示,其中P端通入CO2。
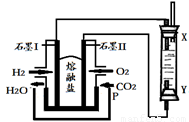
①石墨I电极上的电极反应式为 。
②通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是 (填序号)。
A.X、Y两端都必须用铁作电极
B.可以用NaOH溶液作为电解液
C.阴极发生的反应是:2H2O+ 2e-= H2↑+ 2OH-
D.白色沉淀只能在阳极上产生
③若将所得Fe(OH)2沉淀暴露在空气中,其颜色变化为 ,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015届广东陆丰碣石中学高一下学期第一次月考化学试卷(解析版) 题型:实验题
(I) 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。用FeCl3溶液做腐蚀液与Cu反应生成CuCl2和FeCl2。
(1) 写出该反应的化学方程式 。
(2) 检验溶液中Fe3+存在的试剂是 ,证明Fe3+存在的现象是 。
(Ⅱ) 印刷电路的废腐蚀液含有大量CuCl2、FeCl2、FeCl3,任意排放会造成环境污染及资源的浪费。通过下列流程可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。

⑴ 步骤①中发生反应的离子方程式 。
(2) 步骤②需加入的试剂A是 (填化学式)。
(3) 步骤③通入的气体B是 (填化学式),写出该反应的化学方程式 。
(4) 为测定滤渣中铜的质量分数,取50g的滤渣与足量的试剂A反应,得到5.6L气体(标准状况下),试计算滤渣中铜的质量分数。
查看答案和解析>>
科目:高中化学 来源:2014届云南景洪第一中学高一上期末考试化学试卷(解析版) 题型:实验题
(I)电子工业常用30%的FeCl3。溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。用FeCl3溶液做腐蚀液与Cu反应生成CuCl2和FeCl2。
(1)写出该反应的化学方程式 。
(2)检验溶液中Fe3+存在的试剂是
(Ⅱ)印刷电路的废腐蚀液含有大量CuCl2、FeCl2、FeCl3,任意排放会造成环境污染及资源的浪费。通过下列流程可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。
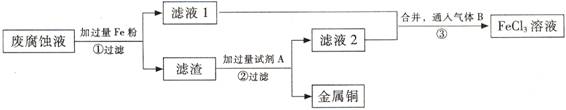 (3) 步骤①中发生反应的离子方程式
(3) 步骤①中发生反应的离子方程式
(4)滤渣的主要成分是 , (填化学式)。
(5)为了除去滤渣中的杂质得到铜,需加入的试剂A是 (填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com