
【题目】铋(Bi)及其化合物广泛应用于电子、医药等领域。一种以含铋矿石辉铋矿(主要成分为Bi2S3,含少量杂质PbO2等)为原料,采用湿法冶金制备铋单质的工艺流程如下:
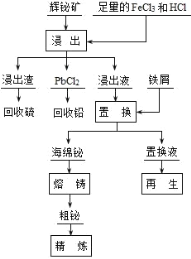
已知:PbCl2是一种难溶于冷水,易溶于热水的白色固体。 回答下列问题:
(1)铋(Bi)位于ⅤA族,铋的氢化物的热稳定性______氨气(填“大于”或“小于”)。
(2)“浸出”时,为了提高浸出速率,可采用的措施有______(任写一条)
(3)加热浸出时,PbO2 生成 PbCl2 和一种气体,此反应的化学方程式为______, 从产物中分离回收 PbCl2 的步骤是______、洗涤、干燥。从保护环境和原料循环利 用的角度,请指出上述工艺流程中可以采取的措施为______。
(4)电解精炼粗铋时必须补充含 Bi3+浓度高的电解液。可用粗铋、铅条作为两个电极,铅条外用素烧 的陶瓷坩埚作隔膜(Bi3+不能透过,H+能透过),电解液开始时为盐酸和食盐的混合液。则粗铋为电解池的 ______极,电解总反应为______。
(5)25℃时,向浓度均为 0.02mol·L-1 的 Cu2+、Bi3+的混合溶液中滴加 Na2S 溶液(设溶液体积增加 1倍),使 Cu2+恰好沉淀完全即溶液中 c(Cu2+)=1×10-5 mol·L-1,此时是否有 Bi2S3 沉淀生成______(列式计算说明)。(已知:25℃时,Ksp(CuS)=6.0×10-36、Ksp(Bi2S3)=1.8×10-99)
【答案】小于 粉碎矿石、搅拌、适当提高浸取液温度 、适当提高溶液浓度等 PbO2 +4HCl![]() PbCl2 + Cl2↑+2H2O 冷却、过滤 “浸出”时生成的氯气,通入置换液中生成三氯化铁循环利用 阳
PbCl2 + Cl2↑+2H2O 冷却、过滤 “浸出”时生成的氯气,通入置换液中生成三氯化铁循环利用 阳  Qc(Bi2S3)=(0.01)2×(6.0×10-36÷1×10-5)3=2.16×10-95> Ksp(Bi2S3)= 1.8×10-99,故有Bi2S3沉淀生成
Qc(Bi2S3)=(0.01)2×(6.0×10-36÷1×10-5)3=2.16×10-95> Ksp(Bi2S3)= 1.8×10-99,故有Bi2S3沉淀生成
【解析】
辉铋矿(主要成分是Bi2S3、还含PbO2杂质)制备铋酸钠,辉铋矿加入氯化铁溶液和盐酸溶解后过滤,氯化铁氧化硫离子为硫单质:Bi2S3+6FeCl3=2BiCl3+6FeCl2+3S,盐酸是防止FeCl3及BiCl3水解生成不溶性沉淀,所以得到滤渣为S,滤液中含有Bi3+,H+,Pb2+,滤液冷却结晶可以得到PbCl2,然后回收铅;再次过滤得到的滤液中加入铁粉过滤得到海绵铋,置换液主要是氯化亚铁;对海绵铋进行熔铸、精炼得到金属铋;置换液中再通入氯气得到氯化铁溶液可以循环使用。
(1)同周期,从上往下,氢化物的稳定性逐渐降低,故铋的氢化物的热稳定性小于氨气;
(2)为了提高浸出率,可采取的措施有将矿石粉粹、搅拌,以增大接触面接,也可适当增大氯化铁溶液的浓度、适当升高温度等;
(3)浸出时,PbO2 生成PbCl2,Pb的化合价降低,则浸出液中HCl化合价升高生成Cl2,化学方程式为PbO2+4HCl=PbCl2+Cl2↑+2H2O;由于PbCl2难溶于冷水,易溶于热水,可对滤液进行冷却结晶然后过滤分离回收PbCl2;置换液为FeCl2,可将浸出时产生的Cl2通入置换液中,使FeCl2转化为FeCl3循环利用,同时防止污染环境;
(4)电解时金属铋需要被氧化生成Bi3+,电极池中阳极得电子发生氧化反应,所以粗铋为电解池的阳极;阴极得电子发生还原反应,根据电解质溶液中的离子种类可知阴极应是氢离子得电子生成氢气,所以电解总反应为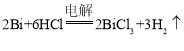 ;
;
(5)Cu2+恰好沉淀完全即溶液中c(Cu2+)=1×10-5molL-1,则此时溶液中c(S2-)=![]() ,此时Qc(Bi2S3)=0.012×(
,此时Qc(Bi2S3)=0.012×(![]() )3=2.16×10-95>Ksp(Bi2S3)=1.8×-99,故有Bi2S3沉淀生成。
)3=2.16×10-95>Ksp(Bi2S3)=1.8×-99,故有Bi2S3沉淀生成。


科目:高中化学 来源: 题型:
【题目】实验室可以用苯乙酮间接电氧化法合成苯甲酸,原理如图所示,下列说法正确的是( )
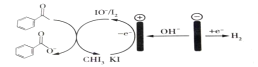
A.这个装置是将化学能转化为电能
B.阴极反应是2H++2e═H2↑
C.阳极I-失去电子后的产物与OH-反应的离子方程式为I2+2OH-=I-+IO-+H2O
D.此装置需要定期向电解质溶液中添加KI溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物F可作为内燃机的润滑油,聚合物![]() (
(![]() )用于制备水凝胶,它们的合成路线如下:
)用于制备水凝胶,它们的合成路线如下:
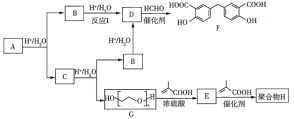
已知:![]() +(n-1)H2O
+(n-1)H2O
nCH2=CH2+nCH2=CHCH3![]()
![]()
(1)![]() 的分子式为
的分子式为![]() ,
,![]() 的化学名称是_________。红外光谱测定结果显示,
的化学名称是_________。红外光谱测定结果显示,![]() 中不含羟基。
中不含羟基。![]() 的反应类型是_____________。
的反应类型是_____________。
(2)![]() 的化学方程式是__________________。
的化学方程式是__________________。
(3)反应![]() 的另一种产物是
的另一种产物是![]() ,其相对分子质量是60,
,其相对分子质量是60,![]() 均能与
均能与![]() 溶液反应产生
溶液反应产生![]() 。
。
①![]() 的结构简式是_______________________。
的结构简式是_______________________。
②![]() 的化学方程式是________________________。
的化学方程式是________________________。
(4)下列说法正确的是_________________。
a.![]() 中均含有酯基
中均含有酯基
b.![]() 中所有碳原子一定在同一平面上
中所有碳原子一定在同一平面上
c.![]() 的同分异构体中能使
的同分异构体中能使![]() 溶液显色的共有1l种
溶液显色的共有1l种
(5)写出由乙烯和甲苯合成![]() 的路线:______________(其他试剂任选)。
的路线:______________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】巨豆三烯酮(F)是一种重要的香料,其合成路线如下:
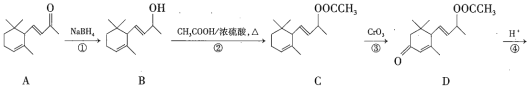
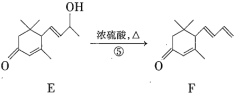
(1)化合物F的分子式为_____________,1mol该物质完全燃烧需消耗________molO2。
(2)在上述转化过程中,反应②的目的是______________,写出反应②的化学方程式:_______________。
(3)下列说法正确的是___________(填序号)。
A.化合物A~F均属于芳香烃的衍生物 B.反应①属于还原反应
C.1mol化合物D可以跟4molH2发生反应 D.化合物F中所含官能团的名称为碳碳双键、羰基
(4)符合下列条件的D的同分异构体有两种,其中一种同分异构体的结构简式如下图所示,请写出另一种同分异构体的结构简式:__________________。
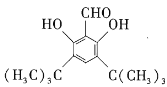
a.属于芳香化合物 b.核磁共振氢谱显示,分子中有4种不同类型的氢原子
c. 1mol该物质最多可消耗2mol NaOH d.能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知卤代烃中卤素原子很容易发生取代反应,如:①R-X+NaCN![]() R-CN+NaX;②2R-X+2Na+X-R′
R-CN+NaX;②2R-X+2Na+X-R′![]() R-R′+2NaX。根据图中各物质的转化关系回答问题:
R-R′+2NaX。根据图中各物质的转化关系回答问题:
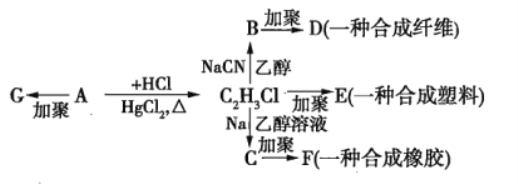
(1)![]() 的分子式为___________,
的分子式为___________,![]() 的结构简式为___________。
的结构简式为___________。
(2)写出![]() 的化学方程式:________。
的化学方程式:________。
(3)写出![]() 的化学方程式:____________。
的化学方程式:____________。
(4)写出![]() 的化学方程式:_____________。
的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知磷酸分子(![]() )中的三个氢原子都可以与重水分子(D2O)中的 D 原子发生氢交换。又知次磷酸( H3 PO2)也可与 D2O 进行氢交换,但次磷酸钠(NaH2PO2)却不能与 D2O 发生氢交换。下列说法正确的是
)中的三个氢原子都可以与重水分子(D2O)中的 D 原子发生氢交换。又知次磷酸( H3 PO2)也可与 D2O 进行氢交换,但次磷酸钠(NaH2PO2)却不能与 D2O 发生氢交换。下列说法正确的是
A.H3 PO2 属于三元酸B.NaH2PO2 溶液可能呈酸性
C.NaH2PO2 属于酸式盐D.H3 PO2 的结构式为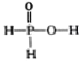
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在CH3COONa溶液里,加入下列物质使水解平衡向左移动,并且pH变大的是 ( )
A. 加入适量纯CH3COOH
B. 加入少量NaCl固体
C. 加入少量NaOH固体
D. 加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞(J)是用于脑血管疾病治疗的药物。它的某种合成路线如下:
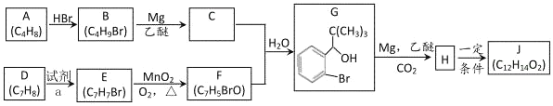
已知: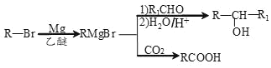
请回答下列问题:
(1)E 的名称为________,F 中所含官能团名称为_______,H→J 的反应类型为_______。
(2)B 生成 A 的方程式_______。
(3)X 是 H 的同系物,相对分子质量比 H 小 56。满足下列条件 X 的同分异构体共有_______种。
①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应。 其中核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式为_______。
(4)利用题中信息所学知识,写出以甲烷和苯甲醛为原料,合成苯乙烯的路线流程图(其他无机试 剂自选)_______。合成路线流程图表达方法例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞(J)是用于脑血管疾病治疗的药物。它的某种合成路线如下:

已知:
请回答下列问题:
(1)E 的名称为________,F 中所含官能团名称为_______,H→J 的反应类型为_______。
(2)B 生成 A 的方程式_______。
(3)X 是 H 的同系物,相对分子质量比 H 小 56。满足下列条件 X 的同分异构体共有_______种。
①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应。 其中核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式为_______。
(4)利用题中信息所学知识,写出以甲烷和苯甲醛为原料,合成苯乙烯的路线流程图(其他无机试 剂自选)_______。合成路线流程图表达方法例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com