
【题目】下列分子中所有原子都满足最外层8电子结构的是
A. PCl3 B. PCl5 C. CH4 D. H2O
 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】下列离子在溶液中可以大量共存的一组是( )
A.H+、Na+、OH﹣
B.Na+、NO3﹣、Cl﹣
C.K+、H+、HCO3﹣
D.Ca2+、SO42﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g) + bB(g)![]() xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )

A.反应物A的百分含量
B.平衡混合气中物质B的百分含量
C.平衡混合气的密度
D.平衡混合气的平均摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2、CS2、COS是由C、O、S三种元素形成的结构相似的化合物。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是 (填序号)
a.亚硫酸溶液加入Na2CO3溶液中,产生气泡
b.氧化性:浓H2SO4>H2CO3
c.CS2中碳元素为+4价,硫元素为﹣2价
d.SO2有较强还原性,而CO2无还原性
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。
①羰基硫的结构式为: 。沸点:CO2_____COS(填“大于”或“小于” ),说明原因________。
②下列有关羰基硫的推测肯定不正确的是
A.COS分子中,所有原子都满足8电子的稳定结构
B.COS分子是含有极性键的非极性分子
C.COS分子中三个原子处于同一直线上
D.COS可能在O2中燃烧
③羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下图:

已知A是一种盐,则A的化学式为 ;气体单质a为 。
(3)在恒容密闭容器中,CO和H2S混合加热生成羰基硫的反应为CO(g)+H2S(g)![]() COS(g)+H2(g),反应前CO和H2S的物质的量均为10 mol,平衡后CO的物质的量为8 mol,回答下列问题:
COS(g)+H2(g),反应前CO和H2S的物质的量均为10 mol,平衡后CO的物质的量为8 mol,回答下列问题:
①升高温度,H2S浓度增加,表明该反应是___________________反应(填“放热”或“吸热”)。
②平衡时,继续通入CO 10 mol和H2S 10 mol,一段时间后再次达到平衡,此时H2S的转化率______(填“增大”“减小”“或”“不变“)。
(4)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是
a.容器内气体密度保持不变
b.CO、H2S、COS、H2的浓度均不再变化
c.c(H2)=c(H2S)
d.υ(H2)正=υ(H2S)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A、B、C结构如下:
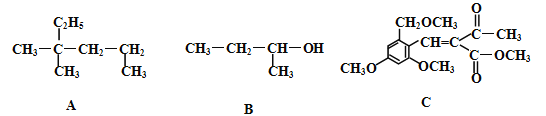
(1)A分子的主链上有 个碳原子 ;若A是某单烯烃与H2发生加成反应后得到的产物,符合此条件的单烯烃有 种。
(2)B在常温下呈 态;B的系统命名法名称是 。
(3)C的分子式是 ,向C中滴入溴水时,1molC能与 molBr2发生加成。
(4)关于A、B、C三种物质的下列说法中不正确的是 。
a.都能发生氧化反应
b.都能发生消去反应
c.都能发生取代反应
d.都能发生聚合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据碘与氢气反应的热化学方程式,下列判断正确的是
(i)H2(g)+ I2(g)![]() 2HI(g);△H= -9.48kJ/mol
2HI(g);△H= -9.48kJ/mol
(ii)H2(g)+ I2(s)![]() 2HI(g);△H= +26.48kJ
2HI(g);△H= +26.48kJ
A.1 mol I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.1 mol I2(s)升华,吸热17.00 kJ
![]() C.反应(i)的产物比反应(ii)的产物稳定
C.反应(i)的产物比反应(ii)的产物稳定
D.反应(ii)的反应物总能量比反应(i)的反应物总能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可由乙苯生产苯乙烯: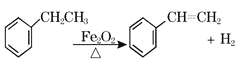 ,下列说法正确的是( )
,下列说法正确的是( )
A. 该反应的类型为消去反应
B. 乙苯的同分异构体共有三种
C. 可用Br2/CCl4鉴别乙苯和苯乙烯
D. 乙苯和苯乙烯分子内共平面的碳原子数均为7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将m g的镁、铜合金加到一定量的稀硝酸中,金属完全溶解(假设反应中还原产物全部是NO).向反应后溶液中加入5mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金质量增加10.2g,则下列叙述正确的是( )
A.当金属全部溶解时,无法计算出参与反应的硝酸的物质的量
B.7.2<m<19.2
C.当金属全部溶解时,收集到NO气体的体积一定为4.48L
D.当生成沉淀的量达到最大值时,消耗NaOH溶液的体积为120mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com