

| A. | 容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) | |
| B. | 保持其他条件不变,升高温度,反应的化学平衡常数K减小 | |
| C. | 反应进行的前3 min内,用X表示的反应速率 v(X)=0.2mol•(L•min)-1 | |
| D. | 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
分析 A、根据物质的量的变化量与化学计量数成正比书写化学方程式;
B、根据图2中曲线的斜率大小判断温度的高低;
C、根据3min内X的物质的量浓度的变化量计算化学反应速率;
D、图3与图1比较,判断平衡是否发生移动,根据影响平衡移动的因素判断.
解答 解:A、根据图1分析,反应中X、Y的物质的量逐渐减小,Z的物质的量逐渐增大,所以X、Y为反应物,Z为生成物,由于该反应反应物没有完全反应,该反应为可逆反应,根据物质的量的变化量与化学计量数成正比可知0.4mol:0.2mol:0.4mol=3:1:2,所以反应的化学方程式为3X(g)+Y(g)?2Z(g),故A正确;
B、根据图2中曲线的斜率大小判断,T2时先到达平衡状态,说明反应速率大,根据温度越高反应速率越大说明T2温度高,温度升高时Y的百分含量降低,说明平衡向正反应方向移动,则平衡常数增大,故B错误;
C、反应进行的前3min内,v(X)=$\frac{0.6mol}{2L×3min}$=0.1mol/(L•min),故C错误;
D、图3与图1比较,图3到达平衡所用的时间较短,说明反应速率增大,但平衡状态没有发生改变,应是加入催化剂所致,故D正确.
故选BC.
点评 本题考查化学平衡移动以及平衡图象题,做题时注意分析图象中曲线的变化规律,结合外界条件对平衡移动的影响进行分析,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ③④⑤⑦⑧ | B. | ③⑥⑦ | C. | ③⑥⑦⑧ | D. | ①②③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属元素原子最外层电子数越少,该金属失电子能力越强 | |
| B. | 铅位于周期表中金属和非金属的交界处,可作半导体材料 | |
| C. | aA2+、bB+、cC3-三种离子具有相同的电子层结构,则原子序数c>a>b | |
| D. | 若存在简单阴离子R2-,则R一定位于ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大理石与醋酸反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| B. | 硅与NaOH溶液反应:Si+2OH-+H2O═SiO32-+2H2↑ | |
| C. | 水玻璃与醋酸反应:SiO32-+2H+═H2SiO3↓ | |
| D. | 硅石与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2能支持燃烧 | |
| B. | NO2不能支持燃烧 | |
| C. | 木条复燃是因为硝酸铜分解产生了氧气的缘故 | |
| D. | 木条复燃是因为硝酸铜分解产生了CuO催化作用的结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
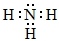 ;
;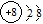 ;它的一种同素异形体是O3.(写化学式)
;它的一种同素异形体是O3.(写化学式)查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 它是一种共价化合物 | B. | 在加热时此化合物可以分解 | ||
| C. | 这种化合物不能跟碱发生反应 | D. | 该化合物可以由PH3跟HI化合而成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com