
设阿伏伽德罗常数为NA,则下列说法正确的是( )
|
| A. | 常温下,2.7g铝与足量的氢氧化钠溶液反应失去的电子数为0.1NA |
|
| B. | 100mL1mol/LNa2SO4溶液中含Na+个数为0.1NA |
|
| C. | 1.7gNH3中含电子数为NA |
|
| D. | 11.2gCO2与8.5gNH3所含分子数都是0.5NA |
考点:
阿伏加德罗常数.
分析:
A.铝为3价金属,2.7g铝的物质的量为0.1mol,完全反应0.1mol铝失去0.3mol电子;
B.Na2SO4中含有2个钠离子;
C.氨气分子中含有10个电子,1.7g氨气的物质的量为0.1mol,含有1mol电子;
D.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算二氧化碳的物质的量.
解答:
解:A.2.7g铝的物质的量为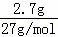 =0.1mol,0.1mol铝完全反应失去0.3mol电子,失去的电子数为0.3NA,故A错误;
=0.1mol,0.1mol铝完全反应失去0.3mol电子,失去的电子数为0.3NA,故A错误;
B.100mL1mol/LNa2SO4溶液中含Na+个数为0.1L×1mol/L×2=0.2mol,即0.2NA个,故B错误;
C.1.7g氨气的物质的量为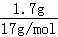 =0.1mol,0.1mol氨气含有的电子数为0.1mil×10=1mol,即NA个,故C正确;
=0.1mol,0.1mol氨气含有的电子数为0.1mil×10=1mol,即NA个,故C正确;
D.不是标况下,无法计算11.2L二氧化碳的物质的量,故D错误;
故选C.
点评:
本题考查阿伏伽德罗常数的应用及计算,难度中等.注意明确标况下气体摩尔体积的使用条件.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
下列物质在水溶液中电离,其电离方程式错误的是( )
|
| A. | Al2(SO4)3=2Al3++3(SO4)2﹣ | B. | NaHSO4=Na++H++SO42﹣ |
|
| C. | MgCl2=Mg2++Cl2﹣ | D. | Ba(OH)2=Ba2++2OH﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
2007年10月党的十七大报告中提到:形成节约能源和保护生态环境的产业结构是人类与自然和谐发展的重要保证,你认为下列行为中有悖于这一保证的是( )
|
| A. | 开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料 |
|
| B. | 研究采煤、采油新技术,提高产量以满足工业生产的快速发展 |
|
| C. | 在农村推广使用沼气 |
|
| D. | 减少资源消耗、增加资源的重复使用和资源的循环再生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 凡是物质的化学变化都伴随着能量的变化 |
|
| B. | 凡是伴随能量变化的都是化学变化 |
|
| C. | 凡是放热反应都需要加热 |
|
| D. | 凡是放热反应都不需要加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中不正确的是( )
|
| A. | 常用铝盐溶液与氨水反应制取氢氧化铝 |
|
| B. | 澄清石灰水盛装在用玻璃塞塞紧的试剂瓶中 |
|
| C. | 氢气在氯气中燃烧产生苍白色火焰 |
|
| D. | 新制氯水通常保存在棕色试剂瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定质量的某有机物和足量钠反应,可得VaL气体,等质量的该有机物如果与足量小苏打反应,同温同压得到VbL气体,若Va=Vb,则该有机物可能是( )
|
| A. | HOCH2COOH | B. | HO﹣CH2CH2﹣CHO |
|
| C. | HOOC﹣COOH | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学上常用燃烧法确定有机物的组成.如图装置是用燃烧法确定烃或烃的含氧衍生物分子式的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成.
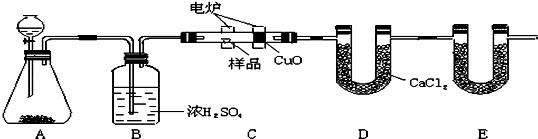
回答下列问题:
(1)装置A中装有MnO2,写出A装置中发生反应的化学方程式是 ;
(2)C装置(燃烧管)中CuO的作用是 ;
(3)写出E装置中所盛放物质的名称 ,它的作用是 .
(4)若将B装置去掉会对实验结果造成什么影响? .
(5)若准确称取1.20g样品(烃或烃的含氧衍生物).经充分燃烧后,E管质量增加1.76g,D管质量增加0.72g,则该有机物的实验式为 .
(6)从定量测定准确角度去考虑,该装置应怎样进一步改进 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com