
| A. |  | B. | 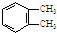 | C. | 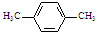 | D. | 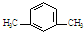 |
分析 苯的同系物苯环上一溴取代物的同分异构体的种数取决于在苯环上甲基的位置决定苯环上氢原子的异同,解题方法是找准对称轴,进行正确判断.
解答 解: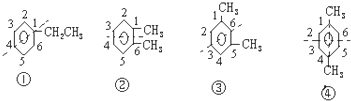 A.对称轴的位置如图①所示,在乙苯中,2、6两个碳原子和3、5两个碳原子分别关于对称轴对称,而第4个碳原子又是另一类不同的碳原子,所以在乙苯中,苯环上的一溴代物有三种同分异构体,故A错误;
A.对称轴的位置如图①所示,在乙苯中,2、6两个碳原子和3、5两个碳原子分别关于对称轴对称,而第4个碳原子又是另一类不同的碳原子,所以在乙苯中,苯环上的一溴代物有三种同分异构体,故A错误;
B.邻二甲苯的一溴代物有两种同分异构体,对称轴分别如图②,故B正确;
C.对二甲苯的一溴代物的同分异构体只有一种,对称轴分别如图④,故C错误;
D.间二甲苯的一溴代物的同分异构体有三种,对称轴分别如图③,故D错误.
故选:B.
点评 本题考查苯的同系物苯环上一溴取代物的同分异构体的种数,题目难度中等,注意解题方法是找准对称轴,进行正确判断.


科目:高中化学 来源: 题型:选择题
| A. | 将0.1mol/L氨水与0.1 mol/L稀盐酸等体积混合:c(NH4+)>c(Cl-)>c(H+)>c(OH-) | |
| B. | 将pH=2 的稀盐酸与pH=12的氨水等体积混合,所得溶液pH>7 | |
| C. | 0.10 mol•L-1的氨水用HNO3溶液完全中和后,溶液显中性 | |
| D. | 用惰性电极电解稀硫酸时,实质是电解水,溶液的pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属性:S>Cl>F | B. | 碱性:NaOH>Mg( 0H)2>Al( 0H)3 | ||
| C. | 稳定性:PH3<H2S<HF | D. | 离子半径:02->Na+>Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b | B. | b>a | C. | a=b | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X的某种单质是一种新型自来水消毒剂 | |
| B. | 简单离子半径:W->R2->X2->S3+ | |
| C. | R、Z不可能形成离子化合物 | |
| D. | 字母所代表的元素中最高价氧化物的水化物酸性最强的是Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com