
【题目】中华民族有着光辉灿烂的发明史,下列发明创造不涉及氧化还原反应的是
A. 火法炼铜B. 转轮排字C. 粮食酿酒D. 钻木取火
科目:高中化学 来源: 题型:
【题目】元素的性质呈周期性变化的根本原因是( )
A. 元素原子量的递增,量变引起质变
B. 元素的原子半径呈周期性变化
C. 元素原子的核外电子排布呈周期性变化
D. 元素的金属性和非金属性呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关卤族元素的叙述不正确的是( )
A. 卤素单质从F2到I2,颜色加深,熔沸点升高
B. 卤族元素从Cl到I,最高价氧化物对应水化物的酸性减弱
C. 卤族元素从F到I, HX水溶液酸性增强
D. 卤素单质氧化性F2>Cl2>Br2>I2,因此排在前面的卤素单质均可将排在后面的卤素从它的盐溶液中置换出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500mL有BaCl2和KC1的混合溶液分成5等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含6mol硝酸银的溶液,恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为( )
A.0.1(b﹣2a)molL﹣1
B.10(2a﹣b)molL﹣1
C.10(b﹣a)molL﹣1
D.10(b﹣2a)molL ﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应热的叙述中正确的是
①已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为△H=-241.8 kJ·mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)![]() Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
④已知:
共价键 | C—C | C===C | C—H | H—H |
键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
上表数据可以计算出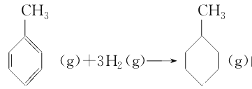 的焓变
的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2固体时,放出的热量相等
⑥25℃,101 kPa时,1 mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
A.①②③④ B.③④⑤ C.④⑤ D.⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】半导体工业中,有一句行话:“从沙滩到用户”,即SiO2制取Si。制取过程中不涉及的化学反应是
A. 2C+SiO2![]() Si+2CO↑
Si+2CO↑
B. SiO2+2NaOH===Na2SiO3+H2O
C. Si+2Cl2![]() SiCl4
SiCl4
D. SiCl4+2H2![]() Si+4HCl
Si+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氢键的下列说法中正确的是( )
A.每个水分子内含有两个氢键
B.在水蒸气、水和冰中都含有氢键
C.分子间能形成氢键使物质的熔点和沸点升高
D.HF的稳定性很强,是因为其分子间能形成氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3═K2O+5Na2O+16N2↑.若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
A.生成42.0 L N2(标准状况)
B.有0.250 mol KNO3被氧化
C.转移电子的物质的量为2.5 mol
D.被氧化的N原子的物质的量为3.75 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述与分子间作用力无关的是 ( )
A.气体物质加压或降温时能凝结或凝固 B.干冰易升华
C.氟、氯、溴、碘单质的熔沸点依次升高 D.氯化钠的熔点较高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com