
300��Cʱ����2 mol A��2 mol B������������2 L�ܱ������У��������·�Ӧ��3A(g)��B(g) 2C(g)��2D(g)����H��Q,2 minĩ�ﵽƽ�⣬����0.8 mol D��
2C(g)��2D(g)����H��Q,2 minĩ�ﵽƽ�⣬����0.8 mol D��
(1)300��Cʱ���÷�Ӧ��ƽ�ⳣ������ʽΪK��________����֪K300��C<K350��C����H________0(�>����<��)��
(2)��2 minĩʱ��B��ƽ��Ũ��Ϊ_______��D��ƽ����Ӧ����Ϊ_______��
(3)���¶Ȳ��䣬��С�����ݻ�����A��ת����________(�������С�����䡱)��ԭ����__________________________________________��
(4)�������ͬ�������£�������Ӧ���淴Ӧ������У���ʼʱ������C��D�� mol����ʹƽ��ʱ�����ʵ����ʵ���Ũ����ԭƽ����ͬ����Ӧ�ü���B________mol��
mol����ʹƽ��ʱ�����ʵ����ʵ���Ũ����ԭƽ����ͬ����Ӧ�ü���B________mol��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����塣��ԭ��Ϊ��
N2(g)��3H2(g) 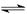 2NH3(g) ��H����92.4 kJ/mol���ݴ˻ش��������⣺
2NH3(g) ��H����92.4 kJ/mol���ݴ˻ش��������⣺
(1)�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK�� ��
�ڸ����¶ȶԻ�ѧƽ���Ӱ����ɿ�֪�����ڸ÷�Ӧ���¶�Խ�ߣ���ƽ�ⳣ����ֵԽ ��
(2)ij�¶��£�����10 mol N2��30 mol H2�������Ϊ10 L���ܱ������ڣ���Ӧ�ﵽƽ��״̬ʱ����û�������а����������Ϊ20%������¶��·�Ӧ��K�� (���÷�����ʾ)����˵���÷�Ӧ�ﵽ��ѧƽ��״̬���� (����ĸ)��
a�������ڵ��ܶȱ��ֲ���
b��������ѹǿ���ֲ���
c��v��(N2)��2v��(NH3)
d�����������c(NH3)����
(3)���ںϳɰ���Ӧ���ԣ������й�ͼ��һ����ȷ����(ѡ�����) ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
һ���¶���ij�ݻ��̶����ܱ������м���2 mol A��1 mol B���������·�Ӧ��2A(g)��B(g)  3C(g)��D(s)����H����Q kJ��mol��1(Q��0)������Ӧ�ﵽƽ���Ӧ�ų�������ΪQ1 kJ������A��ת����Ϊ������ش��������⣺
3C(g)��D(s)����H����Q kJ��mol��1(Q��0)������Ӧ�ﵽƽ���Ӧ�ų�������ΪQ1 kJ������A��ת����Ϊ������ش��������⣺
(1)Q1________Q(�����������������)��������__________________________��
(2)A��ת���ʦ���________(�ú�Q��Q1�Ĵ���ʽ��ʾ)��ƽ�����������������D��A��ת���ʻ�________(���������С�����䡱)��
(3)��Ӧ�ﵽƽ����������¶ȣ�K________(���������С�����䡱)����������ƽ����Է�������________(���������С�����䡱)��
(4)ά���¶Ȳ��䣬����ʼʱ�������м���������������ĸ�ѡ���Ӧ�ﵽƽ���ų���������ΪQ1 kJ����(ϡ�����岻���뷴Ӧ)________(����ĸ)��
A��2 mol A��1 mol B��1 mol Ar
B��3 mol C��1 mol D
C��1 mol A��0.5 mol B��1.5 mol C��0.5 mol D
D��2 mol A��1 mol B��1 mol D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij��糧������β��ͨ�뱥��K2CO3��Һ���ճغ��ֽ���Ƶô�����CO2�����ںϳ�����H2��Ӧ���ɼ״����乤��������ʾ��ͼ����:
��1�����ճ��б���K2CO3��Һ����CO2�����ӷ���ʽ�� ��
��2������ʾ��ͼ��ѭ��ʹ�õ������� ��
��3��300��ʱ���ϳ����еķ�ӦΪCO2(g)��3H2(g) CH3OH(g)��H2O(g)�����ܱ������£�����ʾ��ͼ��˵����Ӧ���е�t1ʱ��ʱ�ﵽƽ��״̬���� (����ĸ���)
CH3OH(g)��H2O(g)�����ܱ������£�����ʾ��ͼ��˵����Ӧ���е�t1ʱ��ʱ�ﵽƽ��״̬���� (����ĸ���)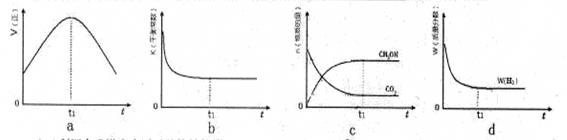
��4�����úϳ�����ʧ���ĸ�п��ý���Ƶú���Cl- ��CrO42- ����Һ����Ũ�Ⱦ�Ϊ0.01mol/L�������Һ����μ���0.01mol/L��AgNO3��Һʱ�����Ȳ����������������� (��֪:Ksp(AgCl)=1.56��10-10��Ksp(Ag2CrO4)=9.0��10-12)
��5���ϳ�����ʧ��ĸ�п��ý�������Ʊ�п�̵�ء��ڼ��������£��õ�ص��ܷ�ӦΪ��Zn(s) ��2MnO2(s) ��H2O(l) = Zn(OH)2(s) ��Mn2O3(s) ���õ�������ĵ缫��Ӧʽ�� �����õ�ص��(���Ե缫)������Mg(NO3)2��NaCl�Ļ����Һ���������������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
Һ����������������ش���������
��1��һ�����������ܱ������з�����Ӧ��
a��NH4I(s)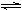 NH3(g) + HI(g) b��2HI(g)
NH3(g) + HI(g) b��2HI(g) 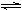 H2(g) + I2(g)
H2(g) + I2(g)
��д����Ӧa��ƽ�ⳣ������ʽ
�ڴﵽƽ������������������Ӧb���ƶ����� ��������������ƶ��������ﵽ�µ�ƽ��ʱ��������ɫ�������仯 ������������dz�����䡱��
��2����ҵ�Ϻϳɰ��ķ�Ӧ��N2(g)��3H2(g) 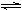 2NH3(g) ��H����92.60 kJ��mol��1
2NH3(g) ��H����92.60 kJ��mol��1
����˵����˵��������Ӧ������Ӧ������е���________(�����)��
a����λʱ��������2n mol NH3��ͬʱ����3n mol H2
b����λʱ��������6n mol N��H����ͬʱ����2n mol H��H��
c����N2��H2��NH3�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����֮��Ϊ1��3��2
d����������ƽ��Ħ����������
e�������ڵ������ܶȲ���
��3����֪�ϳɰ���Ӧ��ij�¶���2 L���ܱ������н��У�����������ݣ�
| ʱ��(h) ���ʵ���(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | | 1.00 | 1.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��һ����NO2��N2O4�Ļ������ͨ�����Ϊ2 L�ĺ����ܱ������У�������Ũ����ʱ��仯�Ĺ�ϵ��ͼ1��ʾ��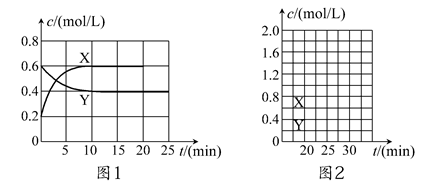
��ش�
(1)ͼl�У�����________(�X����Y��)��ʾNO2Ũ����ʱ��ı仯�����ǰ10 min��v(NO2)��________mol/(L��min)��
(2)����ѡ���в���˵���÷�Ӧ�Ѵﵽƽ��״̬����________(��ѡ����ĸ)��
| A�������ڻ�������ѹǿ����ʱ��仯���ı� |
| B�������ڻ��������ܶȲ���ʱ��仯���ı� |
| C�������ڻ���������ɫ����ʱ��仯���ı� |
| D�������ڻ�������ƽ����Է�����������ʱ��仯���仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������Ҫ�ĵ��ʣ��Dz����ϴ�Ļ�����Ʒ֮һ���α�����ܵĺϳɰ�������Ϊ���������ǵ¹��˹�����1905�귢���ģ���ϳ�ԭ��Ϊ��
N2(g)��3H2(g) 2NH3(g) ��H����92.4 kJ��mol��1
2NH3(g) ��H����92.4 kJ��mol��1
����˻����1918��ŵ������ѧ�����Իش��������⣺
(1)�ϳɰ���ҵ�в�ȡ�����д�ʩ������������ԭ�����͵���________��
| A�����ýϸ�ѹǿ |
| B������500 ��ĸ��� |
| C��������ý������ |
| D�������ɵİ�Һ������ʱ����ϵ�з��������ʣ��N2��H2ѭ�����ϳ��� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��������ʵ�У�ʲô����Ӱ���˻�ѧ��Ӧ�����ʣ�
(1)����ƿ����H2��Cl2�Ļ�����壬��ƿ���ȼþ��ʱ������ը________��
(2)����������ʱҪ�����ϸС�Ŀ���________��
(3)KI�����HgCl2�����Ϻ�������������һ��Ͷ��ˮ�У��ܿ����ɺ�ɫHgI2___________________________��
(4)�ۻ���KClO3�ų����ݺ�������������MnO2��ܿ��������________��
(5)ͬŨ�ȡ�ͬ����������з���ͬ����С��п����þ�飬��������������п�����________��
(6)ͬ����С��ʯ��ʯ�ֱ���0.1 mol��L��1�������1 mol��L��1�������з�Ӧ���ʲ�ͬ________��
(7)�����ʳƷ�ױ�ù������Ͳ�����������__________________________________
(8)�������ڿ�����ȼ��ʱ��Ҫ�ϸߵ��¶ȣ����������������������(37 ��)ʱ���Ϳ��Ա�������������Ϊ______________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����β���к���CO��NO2���ж�����,��������װβ������װ��,��ʹ�ж��������Ӧת��Ϊ�����塣����β����CO��NO2������һ�������¿��Է�����Ӧ:4CO(g)+2NO2(g) 4CO2(g)+N2(g) ��H="-1" 200 kJ��mol-1
4CO2(g)+N2(g) ��H="-1" 200 kJ��mol-1
(1)���º���������,����˵���÷�Ӧ�Ѵﵽƽ��״̬���� (����ĸ,��ͬ)��
A.�����ڻ��������ɫ���ٱ仯
B.�����ڵ�ѹǿ���ֲ���
C.2v(NO2)��=v(N2)��
D.�����ڻ�������ܶȱ��ֲ���
(2)��ʹ�÷�Ӧ�ķ�Ӧ��������,��ƽ�����淴Ӧ�����ƶ����� ��
A.��ʱ�����CO2
B.�ʵ������¶�
C.��С�������ʹ��ϵѹǿ����
D.ѡ���Ч����
(3)���ڸ÷�Ӧ,�¶Ȳ�ͬ(T2��T1)������������ͬʱ,����ͼ����ȷ���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com