
【题目】基本知识填空
(1)在一定条件下,当一个可逆反应的_____与____相等时,反应物的浓度与生成物的浓度不再改变,即达到化学平衡状态。
(2)化学平衡状态的特征:_____、____、_____、_____、_____。
(3)对于可逆化学反应mA+nBpC+qD在一定温度下达到化学平衡时,其平衡常数表达式为:______。
(4)强电解质包括的范围:____、____、____。弱电解质包括的范围:____、_____、____、_____。
【答案】正反应速率 逆反应速率 逆 等 动 定 变 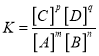 强酸 强碱 大多数盐 弱酸 弱碱 少数盐 水
强酸 强碱 大多数盐 弱酸 弱碱 少数盐 水
【解析】
(1)化学平衡的定义:一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物与生成物的浓度保持不变,达到表面上静止的一种“平衡状态”,这种状态叫化学平衡状态;
(2)化学平衡的特征:①逆:可逆反应;②等:正逆反应速率相等;③动:动态平衡;④定:平衡混合物中百分含量一定;⑤变:改变平衡条件,平衡就会改变,建立新平衡。
(3)平衡常数是平衡时生成物浓度系数次方的乘积与反应物浓度系数次方的乘积的比,对于可逆化学反应mA+nBpC+qD在一定温度下达到化学平衡时,其平衡常数表达式为: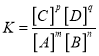 。
。
(4)强电解质是在水溶液中完全电离的化合物,包括的范围:强酸、强碱、大多数盐。弱电解质是在水溶液中部分电离的化合物,包括的范围:弱酸、弱碱、少数盐、水。


科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:
C(s)+2NO(g)![]() CO2(g)+N2(g),平衡时c (NO)与温度T的关系如下图所示,则下列说法正确的是
CO2(g)+N2(g),平衡时c (NO)与温度T的关系如下图所示,则下列说法正确的是
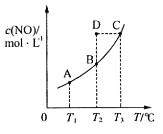
A. 该反应的△H>0
B. 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
C.在T2时,若反应体系处于状态D,则此时![]()
D.若状态B、C、D的压强分别为PB、PC 、PD ,则 PC=PD>PB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年3月21日是第二十七届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关图像如下所示:
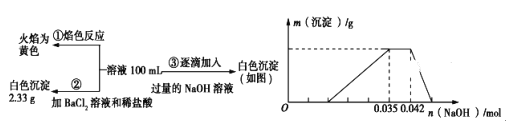
请回答下列问题:
(1)焰色反应是_________ (填“物理”或“化学”)变化;实验②中产白色沉淀是_________ (填化学式)。
(2)原溶液中一定存在的离子有________________,可能存在的离子有________________,一定不存在的离子有________________ (写化学式)。
(3)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为________________
(4)若通过实验确定原废水中c(Na+)=0.14 mol·L1,试判断原废水中NO3是否存在?________________(填“存在”“不存在”或“不确定”)。 若存在,c(NO3)=___________mol·L1。(若不存在或不确定则此空不填)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁是中学常见的物质,其中甲、乙、丙均含有同一种元素,在一定条件下的转化关系如图,下列说法正确的是
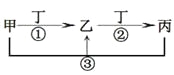
A.若丁为用量最大,用途最广的金属单质,乙的溶液一定为FeCl3
B.若通常情况下甲、乙、丙、丁都是气体,且乙和丁为空气的主要成分,则反应①的化学方程式4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
C.若甲、乙、丙的溶液显碱性,丙可作为医疗上治疗胃酸过多症的药剂,将等物质的量的乙和丙溶于水形成混合溶液,溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)> c(H+)
D.若丁为化合物,且为氯碱工业的重要产品,则甲一定为含Al3+的盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属加工厂排放的污水中含有CuSO4、ZnSO4、FeSO4,某研究小组利用该污水回收工业重要原料硫酸锌和有关金属,其流程如下:
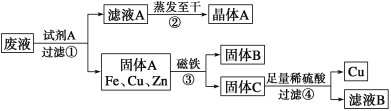
请回答下列问题:
(1)下列说法正确的是________。
A.该工艺流程中发生了3个置换反应
B.CuSO4与Mg(OH)2发生复分解反应可得Cu(OH)2
C.步骤①②③④都包含化学变化
(2)写出步骤①发生反应的离子方程式:__________________、_________________
(3)步骤④中加入足量稀硫酸的目的是________________
(4)滤液B含有的分散质为____________、___________ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学一选修:化学与技术磷矿石主要以[Ca3(PO4)2H2O]和磷灰石[Ca5F(PO4)3,Ca5(OH)(PO4)3]等形式存在,图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸,图(b)是热法磷酸生产过程中由磷灰石制单质磷的流程:
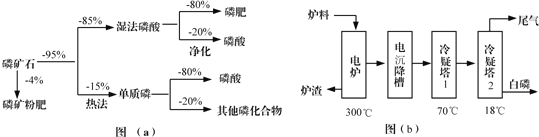
部分物质的相关性质如下:
熔点/℃ | 沸点/℃ | 备注 | |
白磷 | 44 | 280.5 | |
PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
SiF4 | -90 | -86 | 易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的____________;
(2)以磷矿石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为:___________,现有1t折合含有P2O5约30%的磷灰石,最多可制得到85%的商品磷酸___________t。
(3)如图(b)所示,热法磷酸生产过程的第一步是将SiO2、过量焦炭与磷灰石混合,高温反应生成白磷,炉渣的主要成分是___________(填化学式),冷凝塔1的主要沉积物是___________,冷凝塔2的主要沉积物是___________。
(4)尾气中主要含有___________,还含有少量的PH3、H2S和HF等.将尾气先通入纯碱溶液,可除去___________;再通入次氯酸钠溶液,可除去___________(均填化学式)。
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入350mL 2molL﹣1的稀硝酸恰好使混合物完全溶解,放出2.24L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现.若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为( )
A. 0.21 molB. 0.25 molC. 0.3 molD. 0.35 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120℃、101.3 kPa,甲烷(CH4)和过量的O2的混合物,用电火花引燃(CH4+2O2=CO2+2H2O)后,恢复到原来的温度和压强,测得反应后气体密度为相同条件下H2密度的15倍,则原混合气体中甲烷和氧气的体积比为( )
A. 2∶1B. 1∶2C. 1∶7D. 7∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均反应速率分别为( )
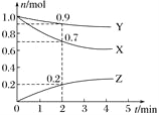
A. X+3Y![]() 2Z 0.1 mol/(L·min) B. 2X+Y
2Z 0.1 mol/(L·min) B. 2X+Y![]() 2Z 0.1 mol/(L·min)
2Z 0.1 mol/(L·min)
C. X+2Y![]() Z 0.05 mol/(L·min) D. 3X+Y
Z 0.05 mol/(L·min) D. 3X+Y![]() 2Z 0.05 mol/(L·min)
2Z 0.05 mol/(L·min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com