
下列说法不正确的是
A.0.1 mol水的摩尔质量为1.8 g/mol
B.1 molH2O的质量等于NA个H2O质量的总和
C.一个12C原子的真实质量为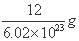
D.1 mol任何物质的质量以克为单位等于该物质的化学式式量
科目:高中化学 来源: 题型:
某温度下,向2 L恒容密闭容器中充入1.0 mol A和1.0 mol B,反应A(g)+B(g)C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
| t/2 | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.反应在前5 s的平均速度v(A)=0.17 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH>0
C.相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
体积相同的甲、乙两份植物营养液,其所含组分的物质的量浓度如下表:
| KCl | K2SO4 | ZnCl2 | ZnSO4 | |
| 甲 | 0.3 mol·L-1 | 0.2 mol·L-1 | 0 | 0.1 mol·L-1 |
| 乙 | 0.1 mol·L-1 | 0.3 mol·L-1 | 0.1 mol·L-1 | 0 |
下列对两份营养液成分的分析中,正确的是( )
A.两种溶液的n(Zn2+)不同 B.两种溶液的c(Cl-)之比为3:1
C.甲溶液的c(K+)=0.5 mol·L-1 D.两种溶液所含的N(SO42-)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
现有含NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-和NO3-的相互分离。相应的实验过程可用下图表示(提示:Na2CO3溶液呈碱性):
|
(1)写出上述实验过程中所用试剂为:
试剂1 ,试剂2 ,试剂4 。
(2)恰当地控制试剂4的加入量的方法是 。
(3)加入过量试剂3的目的是 。
(4)在加入试剂4后,获得固体D的实验操作④是 。(填操作名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数118,中子数为175的超重元素,该元素原子核内中子数与核外电子数之差是( )
A.57 B.47
C.61 D.293
查看答案和解析>>
科目:高中化学 来源: 题型:
I2O5是白色固体,遇水生成碘酸(HIO3)。I2O5可用于检验并定量测定空气中的CO,在常温下发生的反应为 5CO+I2O5=5CO2+I2 (空气中其余气体不与I2O5反应)。
实验一:制取I2O5
将碘酸加热至90~110 ºC使其部分脱水,再升温至220~240 ℃并恒温4 h,使反应完全。接着慢慢冷却至室温,密封保存,即得五氧化二碘。
(1)写出碘酸制I2O5的化学方程式: 。
(2)在制得的I2O5固体中含有少量I2杂质,提纯的方法是 (填标号);
A.过滤 B.蒸发结晶 C.蒸馏 D.升华
该提纯方法用到的玻璃仪器为 (填标号)。
A.圆底烧瓶 B.烧杯 C.普通漏斗 D.酒精灯 E.玻璃棒
实验二:检验空气中CO
 利用右图装置检验空气中是否存在CO。
利用右图装置检验空气中是否存在CO。
(3)能说明空气中含有CO的现象是 。
(4)倘若要从广口瓶中出现浑浊来判断空气中含有CO,请写出改进的实验方案: 。
实验三:测定空气中CO的含量
(5)将I2O5与CO反应生成的碘单质用硫代硫酸钠滴定(反应为I2+2Na2S2O3=Na2S4O6+2NaI),即可根据消耗硫代硫酸钠的量来计算空气中CO的含量。若某次实验时测得参与反应的空气体积为a mL(标准状况下),滴定过程中,共消耗v mL c mol·L-1 Na2S2O3溶液。则该空气样品中CO的体积分数是 。
(6)该实验方案存在的一个明显缺陷是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com