
52 24 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
52 24 |
53 24 |
52 24 |
52 24 |
53 24 |
52 24 |


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
| A、CH3CH2 CH2CH3和CH3CH(CH3)2 |
| B、CH2=C(CH3)2和CH3CH=CHCH3 |
| C、CH3CH2OH和CH3OCH3 |
| D、CH3CH2 CH2COOH 和CH3COOCH2 CH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol H2SO4与 1mol Ba(OH)2完全反应放出的热量叫做中和热 |
| B、等物质的量强酸和弱酸分别与等量的烧碱反应生成等量的水,弱酸反应放出的热量比强酸少 |
| C、CO能继续与O2反应生成稳定的氧化物CO2,所以说CO与O2的反应是吸热反应 |
| D、在101kPa时,1mol C燃烧时放出的热量为C的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2、O2、HBr |
| B、H2、CH4、O2 |
| C、NH3、CO2、HCl |
| D、NH3、O2、N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、符合同一通式的有机物一定互为同系物 |
| B、乙烷不能使溴水和高锰酸钾溶液褪色 |
| C、所有的有机物都很容易燃烧 |
| D、易溶于汽油、酒精、苯等有机溶剂中的物质一定是有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
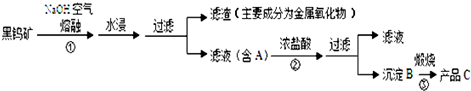
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com