
| ||
| ||
| 光照 |
| 光照 |
| 光照 |
| 光照 |
| 光照 |
| 光照 |
| 光照 |
| 光照 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
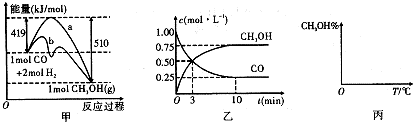
| n(CH3OH) |
| n(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
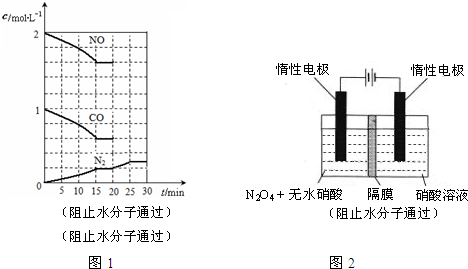
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 一根细如发丝的光缆可以同时传导上千部电话,是铜导线传导能力的约100倍左右.“光缆无铜,盗割有罪”.试问:光缆主要是以
一根细如发丝的光缆可以同时传导上千部电话,是铜导线传导能力的约100倍左右.“光缆无铜,盗割有罪”.试问:光缆主要是以查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇完全燃烧生成CO2和H2O |
| B、乙醇能与水以任意比混溶 |
| C、0.1 mol乙醇与足量钠反应只能生成0.1 g氢气 |
| D、乙醇在铜催化下可被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将金属钠和金属钾混合研磨得到液体 |
| B、刚切开的金属钠放置在空气中变暗 |
| C、刚切开的金属钠放置在空气中加热变成淡黄色 |
| D、一小块钠投入到水中熔成闪亮的小球 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe分别与氯气和稀盐酸反应所得氯化物相同 |
| B、某无色溶液中通入Cl2,溶液变为淡黄色,再加入淀粉溶液,溶液变为蓝色,说明原溶液中存在I- |
| C、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| D、C、N、S三种单质直接与02反应都能生成两种氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com